Vous êtes dans : Accueil > Actualités médicales >
Bradycardie
32 résultats triés par date
affichage des articles n° 1 à 18
La Commission européenne approuve l'ALUNBRIG® (brigatinib) dans le cadre d'un cancer du poumon non à petites cellules ALK chez les patients précédemment traités au crizotinib,...
Takeda Pharmaceutical Company Limited, le 29/11/2018 : Takeda Pharmaceutical Company Limited (TSE: 4502) a annoncé aujourd'hui que la Commission européenne (CE) a accordé une autorisation de mise sur le marché pour l'ALUNBRIG (brigatinib) en tant que monothérapie pour le traitement des patients adultes atteints d'un cancer du poumon non à petites cellules (CPNPC) avancé à kinase positive du lymphome anaplasique (ALK ) ayant précédemment suivi un traitement au crizotinib. La décision fait suite à un avis favorable du Comité des médicaments à usage humain (CHMP) daté du 20 septembre 2018. […].
Takeda présentera un portefeuille croissant et diversifié de produits oncologiques lors de prochains congrès scientifiques
Takeda Pharmaceutical Company Limited, le 20/05/2019 : « Nous sommes impatients de présenter à l'ASCO et à l'AEH des données qui illustrent les progrès continus de notre portefeuille – aussi bien dans le cadre de la recherche clinique qu'en situation réelle – pour les tumeurs solides et les cancers du sang », a déclaré Phil Rowlands, Ph.D., responsable de l’unité thérapeutique Oncologie chez Takeda. « Ces données démontrent notre engagement constant à l'égard de la découverte, du développement et de la distribution de médicaments pour les patients atteints de cancers. » […].
Cancer du poumon : La FDA approuve ALUNBRIG® (brigatinib) de Takeda
Takeda Pharmaceutical Company Limited, le 23/05/2020 : « Nous sommes extrêmement fiers des résultats positifs obtenus par ALUNBRIG pour les patients atteints d’un CPNPC ALK récemment diagnostiqué, en particulier ceux présentant des métastases cérébrales, » a déclaré Teresa Bitetti, présidente, Global Oncology Business Unit, Takeda. « Grâce à son solide programme de développement clinique et aux recherches en cours sur l’ensemble des traitements contre le CPNPC, Takeda s’engage à trouver des solutions pour les personnes atteintes de formes dévastatrices de cancer du poumon, qui ont besoin de nouvelles options thérapeutiques. Nous pensons que l’approbation d’ALUNBRIG est un pas important dans la bonne direction, ainsi qu’un progrès notable pour le portefeuille de traitements contre le cancer du poumon de Takeda. » […].
Takeda va présenter un portefeuille élargi de produits oncologiques, via des présentations de données lors des prochaines réunions médicales
Takeda Pharmaceutical Company Limited, le 28/05/2017 : « La présence de Takeda Oncology à ces prochaines réunions médicales démontre que nous nous efforçons constamment de proposer des innovations aux patients atteints d’un cancer », a déclaré Christophe Bianchi, M.D., président de Takeda Oncology. « Les données que nous présentons soulignent l’intensité et l’ampleur de notre portefeuille récemment élargi, qui inclut dorénavant à la fois les malignités hématologiques et les tumeurs solides, avec la récente homologation d’ALUNBRIG™ (brigatinib) pour le traitement du cancer du poumon non à petites cellules (CPNPC) métastatique, et nous rapproche de notre objectif qui est de guérir le cancer. » […].
Adaptation hémodynamique et cardiovasculaire des cosmonautes en microgravité
Dr L.Labreze, le 15/02/2000 : Le passage de la gravité terrestre à la microgravité s’effectue grâce aux lanceurs modernes en moins de 15 mn. Lors de cette période, les membres d’équipages subissent des accélérations de 3 à 5 G lors de l’allumage des différents étages du lanceur. Ce stress de départ est généralement bien supporté car il est bref et les équipages y sont préparés. […].
Adaptation hémodynamique et cardiovasculaire des cosmonautes en microgravité
Dr L.Labreze, le 15/02/2000 : Le passage de la gravité terrestre à la microgravité s’effectue grâce aux lanceurs modernes en moins de 15 mn. Lors de cette période, les membres d’équipages subissent des accélérations de 3 à 5 G lors de l’allumage des différents étages du lanceur. Ce stress de départ est généralement bien supporté car il est bref et les équipages y sont préparés. […].
Takeda présente les résultats mis à jour de l'essai pivot ALTA de Phase 2 pour l'ALUNBRIGTM (brigatinib) contre le cancer du poumon non à petites cellules ALK positif
Takeda Pharmaceutical Company Limited, le 16/10/2017 : L'étude ALTA randomisée de Phase 2 est conçue pour évaluer l'efficacité et l'innocuité de l'ALUNBRIG avec deux schémas posologiques. Les patients ont soit reçu 90 mg d'ALUNBRIG en prise quotidienne unique (n = 112; 90 mg; groupe A) ou 180 mg en prise quotidienne unique après une période préparatoire de sept jours à 90 mg en prise quotidienne unique (n=110; 180 mg; groupe B). […].
Ipsen annonce la présentation de 16 abstracts relatifs à son portefeuille en oncologie au congrès de l’ESMO
Ipsen, le 04/09/2017 : Ipsen (Euronext : IPN ; ADR : IPSEY) a annoncé aujourd'hui que l'irinotécan liposomal pour injection (Onivyde®), le cabozantinib (Cabometyx®), le lanréotide (Somatuline® Autogel® / Depot), le télotristat éthyl (Xermelo®) et les tumeurs neuroendocrines vont faire l'objet de 16 présentations lors du congrès de l'European Society of Medical Oncology (ESMO 2017), qui se tiendra du 8 au 12 septembre 2017 à Madrid (Espagne). […].
Les autorités réglementaires américaines (FDA) approuvent une nouvelle indication de Somatuline® Depot (lanréotide) Injection d'Ipsen dans le traitement du syndrome carcinoïde
Ipsen, le 18/09/2017 : Ipsen (Euronext : IPN ; ADR : IPSEY) (Ipsen), a annoncé aujourd'hui que les autorités réglementaires américaines (Food and Drug Administration, FDA) ont approuvé une indication supplémentaire (Supplemental new drug application, sNDA) pour Somatuline® Depot (lanréotide) Injection 120 mg dans le traitement du syndrome carcinoïde ; son utilisation permet de réduire la fréquence du recours à des médicaments de secours par un analogue de la somatostatine à courte durée d’action. […].
Pacemakers et épilepsie
Caducee.net, le 21/12/2004 : Les résultats d'une étude anglaise soulignent que le nombre d'interruptions du rythme cardiaque consécutives aux crises d'épilepsie est sous-évalué. Les pacemakers pourraient jouer chez certains patients épileptiques un rôle dans la prévention des morts subites inexpliquées. […].
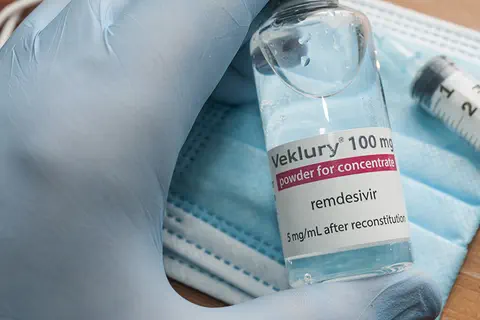
La FDA autorise le Remdesivir (Veklury) dans le traitement de la Covid-19
GILEAD, le 30/10/2020 : Gilead Sciences, Inc. (Nasdaq : GILD) a annoncé le 26 octobre que la Food and Drug Administration (FDA) américaine a autorisé Veklury (remdesivir) pour le traitement des patients atteints de COVID-19 nécessitant une hospitalisation. […].
Insuffisance cardiaque : un système de stimulation cardiaque sans fil prise en charge par le Forfait innovation
EBR Systems, le 22/07/2019 : SUNNYVALE, Californie, 22 juillet 2019 /PRNewswire/ -- EBR Systems, Inc., développeur du seul système de stimulation cardiaque sans fil dans le monde pour insuffisance cardiaque, a annoncé aujourd’hui que la Haute Autorité de santé (HAS) française a décerné à la Société une prise en charge par le Forfait innovation pour son système WiSE™ de thérapie de resynchronisation cardiaque (TRC/CRT). Ce prix pouvant atteindre 1 million d’euros aidera à traiter jusqu’à 40 patients et viendra en appui à l’étude clinique internationale SOLVE CRT. Elle a commencé à recruter en France des patients souffrant d’insuffisance cardiaque au Centre hospitalier universitaire (CHU) Grenoble Alpes, à l’hôpital de la Timone de l’AP-HM (Assistance publique - Hôpitaux de Marseille), au CHU Pontchaillou de Rennes et à la Clinique Pasteur de Toulouse. Les patients ne répondent pas à la TRC ou ne sont pas en mesure de la recevoir. […].
Cancer du sein avancé ER+ , HER2- porteur d'une mutation ESR1 : feu vert de la FDA pour ORSERDU™ (elacestrant)
PRNEWSWIRE, le 01/02/2023 : FLORENCE, Italie et NEW YORK, 1er février 2023 /PRNewswire/ -- Le Goupe Menarini Group (« Menarini »), une société pharmaceutique et de diagnostic italienne de premier plan, a annoncé aujourd'hui que la Food and Drug Administration (FDA) des États-Unis a approuvé ORSERDU™ pour le traitement des femmes ménopausées et des hommes adultes souffrant d'un cancer du sein avancé ou métastatique ER , HER2- porteur d'une mutation ESR1, dont la maladie progresse après au moins une ligne de thérapie endocrinienne. Stemline Therapeutics (« Stemline »), une filiale en propriété exclusive du Groupe Menarini, qui a son siège à New York et se consacre à la fourniture de traitements oncologiques transformationnels pour les patients atteints de cancer, commercialisera ORSERDU™ aux États-Unis. […].
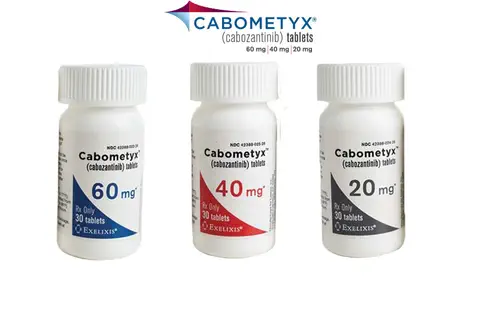
Cancer du rein avancé : CABOMETYX® (cabozantinib) bientôt disponible
Caducee.net, le 30/01/2018 : La filiale française d’Ipsen (Euronext: IPN; ADR: IPSEY) annonce la publication prochaine au Journal Officiel pour CABOMETYX® (cabozantinib) dans le cadre de son Autorisation de Mise sur le Marché (AMM) de son inscription sur la liste des spécialités remboursables aux assurés sociaux ainsi que sur la liste des spécialités agréées à l’usage des collectivités. […].
Ipsen et Exelixis annoncent les résultats de l’étude de phase 3 avec le cabozantinib démontrant un bénéfice significatif en termes de survie globale chez des patients atteints de carcinome hépatocellulaire avancé précédemment traité
Ipsen, le 16/01/2018 : Ipsen (Euronext : IPN ; ADR : IPSEY) et Exelixis, Inc. (NASDAQ : EXEL) ont annoncé aujourd’hui les résultats détaillés de l’étude pivot de phase 3 CELESTIAL chez des patients atteints de carcinome hépatocellulaire (HCC) avancé précédemment traité. Ils seront présentés lors d’une session orale « late-breaking » dans le cadre du Symposium 2018 de l’ASCO-GI qui se tiendra à San Francisco du 18 au 20 janvier 2018. Dans l’étude CELESTIAL, le cabozantinib a démontré une amélioration statistiquement significative de la survie globale (OS) et cliniquement pertinente, par rapport au placebo, critère d'évaluation principal, lors de la deuxième analyse intermédiaire prévue (valeur p critique prédéfinie ≤ 0,021) pour la population de patients en seconde et troisième lignes de traitement inclus dans l’étude. L’OS médiane était de 10,2 mois avec le cabozantinib contre 8,0 mois avec le placebo (HR 0,76, IC 95 % 0,63-0,92 ; p=0,0049). La survie sans progression (PFS) médiane avait plus que doublé, atteignant 5,2 mois avec le cabozantinib et 1,9 mois avec le placebo (HR 0,44, IC 95 % 0,36-0,52 ; p […].
Ipsen et Exelixis présentent les résultats de l'étude de phase 2 CABOSUN comparant le cabozantinib au sunitinib chez des patients atteints d’un carcinome avancé du rein non précédemment traités à l'ESMO 2017
Ipsen, le 09/09/2017 : Ipsen (Euronext : IPN ; ADR : IPSEY) et Exelixis, Inc. (NASDAQ : EXEL) ont annoncé aujourd'hui les résultats actualisés de l'étude randomisée de phase 2 CABOSUN évaluant le cabozantinib chez des patients atteints d’un carcinome avancé du rein (RCC) non précédemment traité, à risque intermédiaire ou élevé selon l'IMDC (International Metastatic Renal Cell Carcinoma Database Consortium). L'investigateur principal, Toni K. Choueiri, M.D., présentera aujourd'hui les données détaillées du late-breaking abstract sur CABOSUN [#LBA38_PD] lors de la séance de présentation de poster Tumeurs génito-urinaires, non prostatiques, à partir de 14h45 CEST (heure locale de Madrid) / 8h45 EDT / 5h45 PDT, dans le cadre du congrès annuel de l'European Society for Medical Oncology (ESMO) 2017, qui se déroule du 8 au 12 septembre 2017 à Madrid en Espagne. […].
Responsabilité médicale : la MACSF observe une hausse record des indemnisations en 2023
Caducee.net, le 26/09/2024 : En 2023, la MACSF a observé une hausse historique des indemnisations en responsabilité médicale, atteignant 62 millions d’euros, malgré une baisse du nombre de décisions judiciaires. Ce bilan met en lumière des spécialités particulièrement à risque, comme la chirurgie et la médecine esthétique, ainsi que des questions émergentes autour de l’intelligence artificielle. […].
L'ANSM fait le point sur le profil de sécurité des quinolones administrées par voie générale
ANSM, le 16/10/2015 : Suite à la persistance de signalements d’effets indésirables connus, l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) souhaite rappeler aux professionnels de santé et aux patients les risques d’effets indésirables des quinolones qui nécessitent une restriction d’utilisation ou une surveillance particulière. […].