Vous êtes dans : Accueil > Actualités médicales >
Risque
4747 résultats triés par date
affichage des articles n° 2521 à 2538
Kyste ou sinus pilonidal
F.Campagne, le 15/05/2000 : Dossier de synthèse Caducée.net sur le kyste ou sinus pilonidal : définition, localisation, symptômes, étiologie, traitements […].
L'onchocercose
E.Faure, le 15/10/1999 : Dossier de synthèse caducee.net sur l'onchocercose : définition, épidémiologie, le cycle parasitaire, traitements et prévention, programmes de lutte contre la maladie. […].
L'onchocercose
E.Faure, le 15/10/1999 : Dossier de synthèse caducee.net sur l'onchocercose : définition, épidémiologie, le cycle parasitaire, traitements et prévention, programmes de lutte contre la maladie. […].
Pourquoi les os des femmes se brisent-ils plus facilement que leur coeur ?
Nutrinews, le 15/07/2002 : Si les femmes sont peut-être plus romantiques que les hommes, leur cœur est indiscutablement plus résistant. En revanche, leur squelette est plus vulnérable et la grande majorité des fractures liées à l'ostéoporose survient chez les femmes. Pourquoi ces spécificités féminines ? C'est ce qu'ont tenté d'expliquer les spécialistes réunis par le CERIN fin octobre à Paris lors du colloque européen "Femmes et Nutrition"*. […].
Pourquoi les os des femmes se brisent-ils plus facilement que leur coeur ?
Nutrinews, le 15/07/2002 : Si les femmes sont peut-être plus romantiques que les hommes, leur cœur est indiscutablement plus résistant. En revanche, leur squelette est plus vulnérable et la grande majorité des fractures liées à l'ostéoporose survient chez les femmes. Pourquoi ces spécificités féminines ? C'est ce qu'ont tenté d'expliquer les spécialistes réunis par le CERIN fin octobre à Paris lors du colloque européen "Femmes et Nutrition"*. […].
Allergies et allergènes alimentaires
INRA, le 01/01/2000 : […].
Allergies et allergènes alimentaires
INRA, le 01/01/2000 : […].
Conférence de presse dans le cadre des entretiens de Bichat
F.Girard, le 01/01/2000 : Le point complet sur conférence de presse dans le cadre des entretiens de bichat : . […].
Conférence de presse dans le cadre des entretiens de Bichat
F.Girard, le 01/01/2000 : Le point complet sur conférence de presse dans le cadre des entretiens de bichat : . […].
Vitamine A : entre besoin physiologique, risque de carence et danger d’excès
Caducee.net, le 01/02/2026 : Longtemps cantonnée, dans l’imaginaire collectif, à la seule santé visuelle, la vitamine A occupe en réalité une place bien plus large dans la physiologie humaine. Elle intervient dans l’immunité, la différenciation cellulaire, le développement embryonnaire et l’entretien des épithéliums. Mais ce nutriment essentiel présente une singularité qui en fait un sujet à double tranchant : la carence continue de peser lourdement dans de nombreuses régions du monde, tandis que, dans les pays à haut revenu, l’attention se déplace davantage vers le risque d’excès, en particulier via les compléments alimentaires et certaines sources très concentrées comme le foie.[1][2][3] […].
Vitamine A : entre besoin physiologique, risque de carence et danger d’excès
Caducee.net, le 01/02/2026 : Longtemps cantonnée, dans l’imaginaire collectif, à la seule santé visuelle, la vitamine A occupe en réalité une place bien plus large dans la physiologie humaine. Elle intervient dans l’immunité, la différenciation cellulaire, le développement embryonnaire et l’entretien des épithéliums. Mais ce nutriment essentiel présente une singularité qui en fait un sujet à double tranchant : la carence continue de peser lourdement dans de nombreuses régions du monde, tandis que, dans les pays à haut revenu, l’attention se déplace davantage vers le risque d’excès, en particulier via les compléments alimentaires et certaines sources très concentrées comme le foie.[1][2][3] […].
Vitamine C : fonctions, carences et place réelle en pratique clinique
Caducee.net, le 01/02/2026 : La vitamine C, ou acide ascorbique, appartient à ces micronutriments dont la notoriété dépasse souvent la réalité clinique. Présentée de longue date comme un réflexe de prévention hivernale, elle continue d’alimenter un imaginaire sanitaire foisonnant, parfois au prix d’un certain flou. Or, lorsque l’on revient aux données disponibles, son intérêt apparaît à la fois net sur le plan physiologique et plus mesuré dans ses applications cliniques courantes. Cette distinction permet justement de sortir des promesses en trompe-l’œil et de replacer la vitamine C à son véritable niveau : celui d’un nutriment indispensable, mais non d’un remède universel.[1][2] […].
Vitamine C : fonctions, carences et place réelle en pratique clinique
Caducee.net, le 01/02/2026 : La vitamine C, ou acide ascorbique, appartient à ces micronutriments dont la notoriété dépasse souvent la réalité clinique. Présentée de longue date comme un réflexe de prévention hivernale, elle continue d’alimenter un imaginaire sanitaire foisonnant, parfois au prix d’un certain flou. Or, lorsque l’on revient aux données disponibles, son intérêt apparaît à la fois net sur le plan physiologique et plus mesuré dans ses applications cliniques courantes. Cette distinction permet justement de sortir des promesses en trompe-l’œil et de replacer la vitamine C à son véritable niveau : celui d’un nutriment indispensable, mais non d’un remède universel.[1][2] […].
Pesticides organochlorés et santé publique aux Antilles françaises
, le 18/09/2007 : L'utilisation des pesticides de la famille des organochlorés (dont le chlordécone) a été intense aux Antilles françaises, en lien avec la culture de la banane. Les risques potentiels pour la santé de ces produits, ainsi que leur grande rémanence dans l'environnement ont entrainé des restrictions d'emploi à partir de 1969, puis leur retrait définitif. Le chlordécone a été définitivement interdit aux Antilles en septembre 1993 (avec un délai dérogatoire de trois ans après l'interdiction en métropole, suite aux dommages entrainés dans les bananeraies par deux cyclones). […].
Recommandations de l’Académie Nationale de Médecine concernant la prise en charge extrahospitalière de l’arrêt cardiocirculatoire
Académie de Médecine, le 30/01/2007 : Les arrêts cardiocirculatoires inopinés sont responsables d’environ 50 000 morts subites par an en France. Plus de la moitié d’entre eux sont liés à une fibrillation ventriculaire. Le taux de survie observé à 1 mois est actuellement inférieur à 3%. Un appel immédiat aux unités mobiles de secours, des manœuvres simples de réanimation à la portée de tous (massage cardiaque externe en particulier), une défibrillation cardiaque très précoce, devraient pouvoir faire passer ce taux de survie à plus de 30%. L’apparition des défibrillateurs entièrement automatiques doit permettre leur utilisation par l’ensemble de la population informée. […].
Traitement hormonal de la ménopause : Actualisation des recommandations et de l’information à destination des femmes
AFSSAPS, le 27/07/2006 : L'Agence française de sécurité sanitaire des produits de santé (Afssaps) vient d'actualiser ses recommandations sur le traitement hormonal de la Ménopause (THM) afin d'y intégrer les nouvelles études et compléments d'études publiés depuis décembre 2003. Des messages-clé et un ensemble de questions/réponses sur le THM ont été élaborés afin d'informer au mieux les femmes. […].
Pour une grande mobilisation nationale de tous les acteurs pour la promotion de la nutrition en France - Eléments de bilan du PNNS (2001-2005) et propositions de nouvelles stratégies pour le PNNS2 (2006-2008)
Ministere de la santé, le 04/04/2006 : Le présent rapport a été rédigé à la demande de Mr Xavier Bertrand, ministre de la santé et des solidarités. Il vise, d'une part, à donner des éléments de bilan tant quantitatif que qualitatif du PNNS (programme national nutrition santé) 2001-2005, et, d'autre part, à proposer des recommandations pour la mise en place de nouvelles stratégies pour la suite du PNNS2 (2006-2008). […].
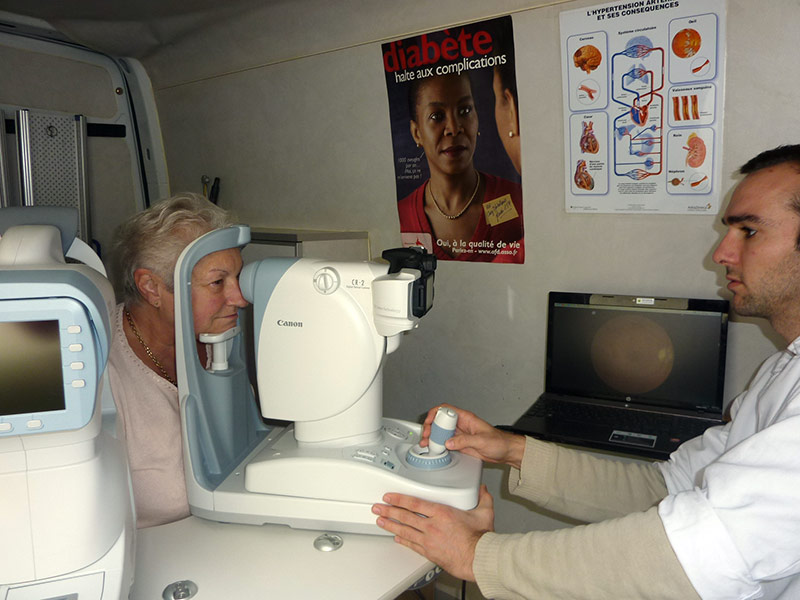
Reprise du dépistage de la rétinopathie diabétique dans l'Yonne à partir du 28 octobre
URPS-Médecins Libéraux de Bourgogne, le 25/10/2014 : 10 ans après son lancement, la campagne de dépistage de la rétinopathie diabétique confirme son succès. Depuis 2004, 10.000 patients ont déjà été dépistés. La campagne de dépistage se poursuit dans l'Yonne jusqu'au 6 novembre (quelques jours avant la Journée Mondiale du Diabète, qui aura lieu le 14 novembre). Le diabète est une épidémie mondiale, qui touche 3,5 millions de personnes en France, - soit 4 % de la population - un nombre qui a doublé en dix ans. […].