Vous êtes dans : Accueil > Actualités médicales >
Essais
2014 résultats triés par date
affichage des articles n° 685 à 702
De nouvelles données sur PLENVU® (NER1006) lors du Congrès de l'ACG montrent un meilleur nettoyage des intestins par rapport à celui obtenu avec des préparations couramment utilisées
Norgine Limited, le 16/10/2017 : AMSTERDAM, October 16, 2017 /PRNewswire/ --Norgine B.V. a présenté aujourd'hui de nouvelles données qui démontrent l'efficacité d'un nettoyage de plus grande qualité des intestins (du moins sur l'un des segments du côlon) de PLENVU® (NER1006) par rapport à deux autres préparations des intestins couramment utilisées : la solution de picosulfate de sodium et de sels de magnésium (CITRAFLEET®) et la solution de 2 litres de polyéthylène glycol (PEG) avec de l'ascorbate (MOVIPREP®). […].
Takeda présente les résultats mis à jour de l'essai pivot ALTA de Phase 2 pour l'ALUNBRIGTM (brigatinib) contre le cancer du poumon non à petites cellules ALK positif
Takeda Pharmaceutical Company Limited, le 16/10/2017 : L'étude ALTA randomisée de Phase 2 est conçue pour évaluer l'efficacité et l'innocuité de l'ALUNBRIG avec deux schémas posologiques. Les patients ont soit reçu 90 mg d'ALUNBRIG en prise quotidienne unique (n = 112; 90 mg; groupe A) ou 180 mg en prise quotidienne unique après une période préparatoire de sept jours à 90 mg en prise quotidienne unique (n=110; 180 mg; groupe B). […].
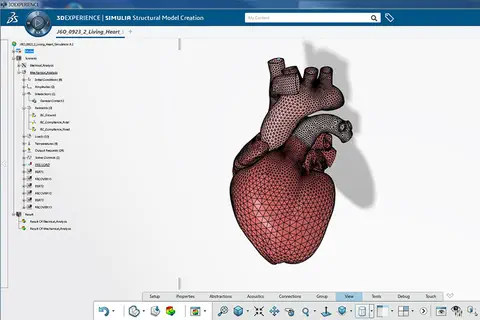
Cœurs personnalisés simulés en 3D : le projet Living Heart de Dassault Systèmes accessible dans le cloud
DASSAULT SYSTEMES, le 19/10/2017 : À l’occasion du 3DEXPERIENCE Forum North America, Dassault Systèmes (Euronext Paris : #13065, DSY.PA) dévoile plusieurs étapes importantes ayant été franchies dans le cadre de son projet Living Heart. […].
AVEO Oncology et EUSA Pharma annoncent des résultats prometteurs de la Phase 1 de l’étude de Phase 1/2 TiNivo sur le tivozanib et le nivolumab dans le traitement du carcinome à cellules rénales
EUSA Pharma, le 06/11/2017 : AVEO Oncology (NASDAQ : AVEO) et EUSA Pharma ont annoncé aujourd’hui la présentation des résultats prometteurs de la phase 1 de TiNivo, une étude multicentrique de phase 1/2 portant sur le tivozanib (FOTIVDA®) en combinaison avec le nivolumab (OPDIVO®) de Bristol-Myers Squibb, un point de contrôle immunitaire, ou PD-1, un inhibiteur, pour le traitement du carcinome à cellules rénales (CCR). Les résultats ont été présentés le vendredi 3 novembre, lors du 16e Symposium international sur le cancer du rein à Miami, dans une présentation orale intitulée « TiNivo : un essai à dose croissante de phase Ib portant sur le Tivozanib et le Nivolumab dans le carcinome à cellules rénales » par Laurence Albiges, M.D., Ph.D., chef de l’unité génito-urinaire de l’Institut Gustave Roussy, et un chercheur principal de l’étude. Une copie de la présentation est disponible à l’adresse www.aveooncology.com ou de plus amples informations peuvent être obtenues via EUSA Pharma Medical Information. […].
Marken lance une nouvelle appli pour les patients cliniques
Marken, le 07/11/2017 : La nouvelle appli smartphone Marken Viseo permet aux patients de suivre leurs livraisons à domicile […].
La French Health Tech pourrait améliorer le quotidien de 11 millions de patients en France et créer 130 000 emplois
FRANCE BIOTECH, le 14/11/2017 : Thérapies innovantes, médecine personnalisée, amélioration de la qualité de vie et optimisation du pilotage du système de santé... les innovations de rupture portées par les start-ups de la Health Tech promettent une véritable révolution. Dans ce contexte, quels sont les atouts et les opportunités pour la French Health Tech ? Pour mieux comprendre ces enjeux, France Biotech présente aujourd'hui une étude prospective réalisée par le BCG et intitulée « La French Health Tech : faire de la France un leader mondial de la santé ». […].
Erelzi ® (étanercept) biosimilaire développé en Europe par Sandoz sera bientôt disponible en France
Caducee.net, le 23/11/2017 : La Commission européenne a autorisé l’utilisation d’Erelzi®, biosimilaire du laboratoire Sandoz, dans le traitement des maladies inflammatoires à médiation immunitaire telles que la polyarthrite rhumatoïde, le psoriasis et l’arthrite psoriasiquei. · Cette AMM offre une nouvelle option thérapeutique aux professionnels de santé et aux patients, et contribue à améliorer l’accès au soin des patients et au financement de l’innovation. · Sandoz, division du groupe Novartis, dispose désormais de cinq médicaments biosimilaires autorisés en Europeii. · Erelzi® est fabriqué en Europe selon le respect rigoureux des standards de qualité […].
Traitement préventif de la migraine : efficacité démontrée d'erenumab (AMG334) dans une étude de phase 3
NOVARTIS, le 30/11/2017 : • Les patients souffrant de migraine épisodique ayant reçu erenumab ont rapporté des bénéfices significatifs durant les six mois de l’étude, notamment une réduction du nombre de jours de migraine et une réduction du recours aux traitements des crises • 50% des patients traités par 140 mg d’erenumab ont vu leur nombre de jours de migraine divisé au moins par deux, avec un odd ratio trois fois plus important que le placebo • Les patients traités par erenumab ont rapporté une réduction de la gêne physique et une amélioration de leur capacité à accomplir les tâches quotidiennes (selon un outil d’auto-évaluation) • Plus de 90% des patients ont terminé l'étude de six mois ; cela vient renforcer les données relatives aux profils de sécurité et de tolérance d’erenumab, données retrouvées tout au long du programme d’études cliniques et comparables au placebo […].
France Biotech présente le Panorama France Health Tech 2017
FRANCE BIOTECH, le 13/12/2017 : France Biotech, l’association des entrepreneurs de l’innovation en santé, (www.france-biotech.fr), publie la quinzième édition du « Panorama France Health Tech », une étude de référence sur ce secteur crucial pour l’économie et la société française. Cette année, 302 entreprises françaises ont participé à cette étude réalisée avec le soutient de BPIFRANCE, KPLG et EURONEXT […].
Recherche : Le CHU de Nantes et le laboratoire Janssen signe un accord-cadre de partenariat
CHU NANTES, le 29/05/2018 : Le CHU de Nantes et le laboratoire Janssen formalisent leur engagement commun en faveur de la recherche clinique et de l’innovation, et mutualisent leurs efforts à travers la signature d’un accord-cadre de partenariat. A travers cette signature, qui a eu lieu le 28 mai dernier, les deux acteurs souhaitent instaurer une collaboration privilégiée en matière de recherche et développement, de recherche clinique et d’amélioration de la prise en charge des patients. […].
VIH : AMM européenne pour le Biktarvy
GILEAD, le 09/07/2018 : La Commission Européenne a accordé le 25 juin dernie rune autorisation de mise sur le marché pour Biktarvy® (bictégravir 50 mg/emtricitabine 200 mg/ténofovir alafénamide 25 mg ; BIC/FTC/TAF), association en comprimé unique en prise unique quotidienne (STR) pour le traitement de l’infection par le VIH-1. […].
Grapevine World annonce un pilote d'échange de données cliniques basé sur la blockchain en collaboration avec l'Université de Southampton et Tiani Spirit
Grapevine World, le 31/07/2018 : VIENNE, July 31, 2018 /PRNewswire/ --Grapevine World est un écosystème décentralisé pour l'échange et l'utilisation fluides de données sur la santé de façon standardisée et sécurisée. En collaboration avec l'Université de Southampton et Tiani Spirit, une nouvelle plateforme basée sur la blockchain utilisant la plateforme cloud de confiance Microsoft Azure pour déterminer la provenance des données sur les soins de santé a été développée pour éliminer les obstacles aux données et simplifier l'accès et la capacité à utiliser les données sur la santé pour les professionnels. […].
Les startups Cureety, Doctoconsult et libheros s’allient pour optimiser et sécuriser le parcours de soins oncologiques
Caducee.net, le 27/11/2018 : Sécuriser le parcours de soins des patients atteints d’un cancer en optimisant la relation ville-hôpital, telle est l’ambition de la startup Cureety. A l’occasion des Rencontres Françaises de la Cancérologie 2018 du 27 au 28 novembre à Paris, Cureety dévoile l’alliance conclue avec Doctoconsult et libheros, deux autres startups complémentaires de l’écosystème eSanté. Les solutions novatrices développées par ces trois startups sont inter-opérées pour proposer une expertise de pointe gratuite à chaque étape du parcours de soins en oncologie pour le patient, Cureety proposant à partir de sa plateforme tous les services connexes de prise en charge des patients atteints de cancer (lien quotidien avec l'hôpital, prise de rendez-vous avec une infirmière à domicile, téléconsultation avec un oncologue). […].
Chirurgie de l’incontinence urinaire d’effort par bandelettes synthétiques sous-urétrales
Caducee.net, le 28/11/2018 : Ce communiqué a pour objectif d’expliquer pourquoi les bandelettes sous-urétrales (BSU) sont souvent la meilleure option dans la prise en charge chirurgicale de l’incontinence urinaire d’effort (IUE), un symptôme gênant qui touche une femme sur trois. […].
La Commission européenne approuve l'ALUNBRIG® (brigatinib) dans le cadre d'un cancer du poumon non à petites cellules ALK chez les patients précédemment traités au crizotinib,...
Takeda Pharmaceutical Company Limited, le 29/11/2018 : Takeda Pharmaceutical Company Limited (TSE: 4502) a annoncé aujourd'hui que la Commission européenne (CE) a accordé une autorisation de mise sur le marché pour l'ALUNBRIG (brigatinib) en tant que monothérapie pour le traitement des patients adultes atteints d'un cancer du poumon non à petites cellules (CPNPC) avancé à kinase positive du lymphome anaplasique (ALK ) ayant précédemment suivi un traitement au crizotinib. La décision fait suite à un avis favorable du Comité des médicaments à usage humain (CHMP) daté du 20 septembre 2018. […].
Therachon obtient une désignation de médicament orphelin par la FDA américaine pour l'apraglutide dans le cadre du traitement du syndrome de l'intestin court
Therachon AG, le 16/01/2019 : Deuxième désignation de médicament orphelin pour l'apraglutide, analogue du GLP-2 synthétique de nouvelle génération offrant potentiellement un profil de premier ordre […].
4D Pharma annonce la publication de données mettant en évidence les propriétés immunostimulantes du MRx0518
4D pharma plc, le 29/01/2019 : LEEDS, Angleterre, January 29, 2019 /PRNewswire/ --4D pharma plc (AIM : DDDD), la société pharmaceutique à la tête du développement de biothérapeutiques vivants, a annoncé aujourd'hui la publication d'un article décrivant le mécanisme et les puissants effets immuno-stimulants du MRx0518. […].
Ipsen s'offre Clementia Pharmaceuticals et renforce son portefeuille dans les Maladies Rares
Ipsen, le 25/02/2019 : Ipsen (Euronext : IPN ; ADR : IPSEY) et Clementia Pharmaceuticals (NASDAQ : CMTA) ont annoncé aujourd’hui avoir conclu un accord en vertu duquel Ipsen se porte acquéreur de la totalité des actions de Clementia Pharmaceuticals, dont la molécule en phase avancée, le palovarotène, un agoniste sélectif du récepteur gamma de l’acide rétinoïque (RARγ), pour le traitement des personnes atteintes de fibrodysplasie ossifiante progressive (FOP), d’ostéochondromes multiples (OM) et d’autres maladies. L’acquisition procédera selon un plan d’arrangement approuvé par la Cour en vertu de la Loi canadienne sur les sociétés par actions. […].