Vous êtes dans : Accueil > Actualités médicales >
République tchèque
75 résultats triés par date
affichage des articles n° 19 à 36
Ipsen acquiert une sélection de produits de santé grand public de Sanofi
Ipsen, le 13/02/2017 : Ipsen (Euronext: IPN; ADR: IPSEY) a annoncé aujourd’hui avoir conclu un accord définitif avec Sanofi (Euronext: SAN; NYSE: SNY) pour acquérir cinq produits de santé grand public dans certains territoires européens. […].
CardioFocus® annonce l'approbation du marquage CE européen de l'Excalibur Balloon™ HeartLight® de nouvelle génération, conçu pour le traitement de la fibrillation auriculaire
CardioFocus, Inc., le 27/09/2017 : MARLBOROUGH, Massachusetts, 27 septembre 2017 /PRNewswire/ -- CardioFocus, Inc. a annoncé aujourd'hui l'approbation du marquage CE européen du ballon Excalibur HeartLight, une technologie de dernière génération conçue pour le traitement de la fibrillation auriculaire (FA). […].
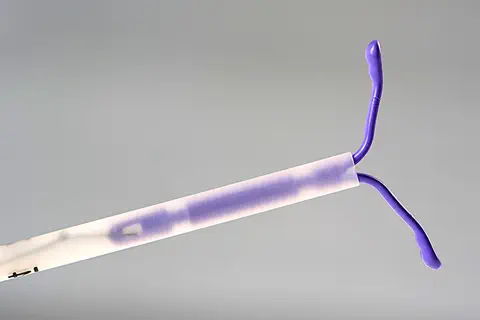
Kyleena, le nouveau système intra-utérin (SIU) de Bayer
BAYER, le 03/05/2018 : Bayer annonce aujourd’hui la mise à disposition de Kyleena® 19,5 mg, un nouveau système de diffusion intra-utérin (SIU) libérant une faible quantité totale de lévonorgestrel (LNG). Après une information éclairée sur les bénéfices et les risques, cette méthode contraceptive hormonale, réversible, de longue durée d’action, peut être proposée aux femmes n’y présentant pas de contre-indications quel que soit leur âge, qu’elles aient eu ou non des enfants, dans le respect des recommandations de l’HAS pour la prescription de contraception […].
CITY HEALTHCARE, Une 5e édition sous le signe de l’Intelligence artificielle et de l’Éthique en Santé
CITY HEALTHCARE, le 05/02/2020 : La cinquième édition du salon sera, cette année encore, l’occasion de découvrir les innovations qui bénéficient aux patients et facilitent la vie des professionnels de santé. L’occasion également de mieux comprendre l’intérêt de l’e-santé, avec le bilan du Tour de France « Ma santé 2022 » (17 régions visitées) et l’expérience du premier service e-santé transfrontalier au Luxembourg, pays invité d’honneur de l’édition 2020. Enfin, l’opportunité d’appréhender les concepts d’IA et d’éthique en santé. […].
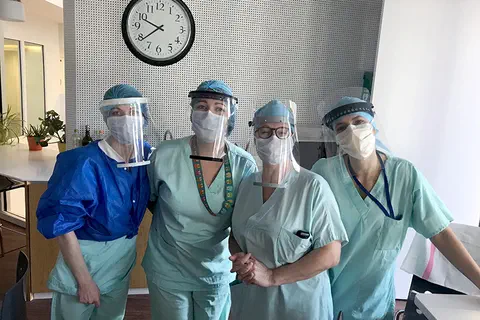
À Strasbourg, la communauté des innovateurs en santé a conçu des boucliers de protection pour les soignants
BoucliersFablab, le 03/04/2020 : Initié par une équipe médicale de Strasbourg, un groupe de travail s’est constitué pour développer des solutions de protection pour les personnes exposées au virus COVID-19. […].
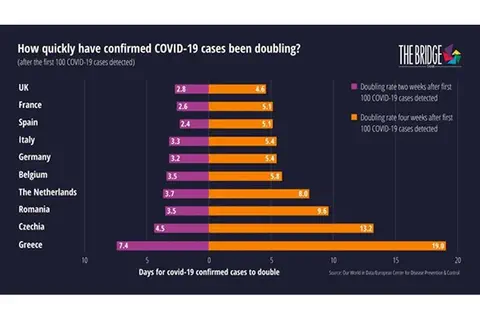
Aplatir la courbe : une analyse comparative paneuropéenne sur la flambée épidémique du COVID-19
PRNEWSWIRE, le 21/04/2020 : PARIS, 16 avril 2020 /PRNewswire/ -- Un nouveau rapport publié par le Bridge Tank compare la flambée épidémique du COVID-19 à travers dix principaux pays européens. […].
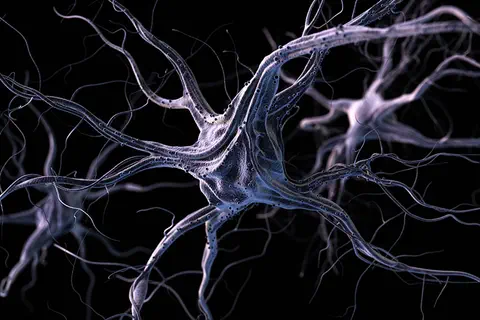
Le coronavirus SARS-CoV-2 peut infecter les neurones selon une étude franco-américaine
Sorbonne Université, le 19/01/2021 : Une étude internationale impliquant plusieurs équipes de l’Université de Yale (USA), de l’Institut du Cerveau (Sorbonne Université/INSERM/CNRS) et de l’hôpital Pitié-Salpêtrière AP-HP confirme la capacité du SARS-CoV-2 à infecter les neurones et en identifie plusieurs conséquences. Les résultats ont été publiés le 12 janvier 2021 dans la revue Journal of Experimental Medicine. […].
BioVaxys et Procare Health annoncent une vaste collaboration pour le développement, la commercialisation et le marketing de vaccins contre le cancer et de vaccins antiviraux
BioVaxys Technology Corp., le 12/02/2021 : VANCOUVER, Colombie-Britannique et BARCELONE, Espagne, 10 février 2021 /PRNewswire/ -- BioVaxys Technology Corp. (CSE: BIOV) (FRA: 5LB) (OTC:L MNGF) (« BioVaxys »), le leader mondial de vaccins à base de protéines hapténisées pour des applications antivirales et anticancéreuses, et Procare Health Iberia, S.L., de Barcelone en Espagne (« Procare Health »), une importante société pharmaceutique privée européenne, ont annoncé aujourd'hui qu'elles avaient engagé une vaste collaboration pour le co-développement, la commercialisation conjointe et le marketing des vaccins BioVaxys contre le cancer des ovaires, le cancer du col de l'utérus et le papillomavirus humain (« PVH »), ainsi que le droit de premier refus pour la commercialisation par BioVaxys aux États-Unis du gel vaginal de Procare Health, Papilocare™, le premier et le seul produit au monde utilisé dans le traitement et la prévention des lésions du col de l'utérus dépendantes du PVH. […].
Fidia annonce que la FDA a désigné ONCOFID®-P comme médicament orphelin pour le traitement du mésothéliome malin, le cancer causé par l'exposition à l'amiante
Fidia Farmaceutici Spa, le 04/08/2021 : - ONCOFID®-P est une conjugaison innovante de l'anticancéreux paclitaxel (taxol) avec l'acide hyaluronique (HA). […].
Une IA pour détecter précocement les maladies pancréatiques lors des écho-endoscopies
Businesswire, le 29/04/2022 : Le groupe Medi-Globe vient de lancer une coopération de recherche pionnière avec l'Institut Hospitalo-Universitaire (IHU) à Strasbourg. L'objectif de la collaboration est de développer le premier logiciel optimisé par IA au monde pour la détection de maladies du pancréas lors d'examens par échographie endoscopique. En tant que partenaire industriel de l'IHU, le groupe Medi-Globe renforce ainsi son rôle en tant que chef de file de l'innovation dans les thérapies et les diagnostics mini-invasifs. […].
L'appareillage de contrôle de continence Vitala(TM) désormais homologué dans l'Union européenne pour une utilisation de type convexe
PR Newswire, le 24/08/2010 : SKILLMAN, New Jersey, August 24, 2010 /PRNewswire/ -- ConvaTec, l'un des leaders mondiaux dans la conception et la commercialisation de technologies médicales innovantes pour les soins communautaires et hospitaliers, a annoncé aujourd'hui que le système de contrôle de continence (Continence Control Device - CCD) Vitala(TM), le nouveau système stomique sans poche non invasif de la société qui offre une continence temporaire aux personnes ayant subi une colostomie, avait reçu l'homologation CE, aux termes de la Directive européenne sur les appareillages médicaux, pour une durée de port journalière de douze heures avec une barrière cutanée convexe. […].
Une meilleure santé est-elle synonyme d'une plus grande richesse?
PR Newswire, le 24/06/2008 : COPENHAGUE et TALLINN, June 24 /PRNewswire/ -- Nous savons depuis longtemps déjà que le fait d'avoir de meilleures ressources financières permet d'effectuer de meilleurs choix en matière de santé. Toutefois, l'inverse est-il également vrai? Une meilleure santé est-elle synonyme d'une plus grande richesse à l'échelle individuelle et nationale ? […].
Rebif(R), médicament de Merck Serono, fête son 10ème anniversaire
PR Newswire, le 10/06/2008 : GENÈVE, Suisse, June 10 /PRNewswire/ -- Rebif(R) (interféron bêta-1a), médicament de Merck Serono, fête cette année son 10ème anniversaire. Depuis l'obtention, il y a 10 ans, de son autorisation de mise sur le marché au sein de l'Union Européenne, ainsi qu'au Canada et en Suisse, pour le traitement des formes rémittentes-récidivantes de sclérose en plaques, Rebif(R) est devenu un traitement majeur de la sclérose en plaques. […].
Resultat positif pour le traitement de l'epilepsie en ecosse - le SMC approuve Zebinix, nouvel anti-epileptique administre une fois par jour
PR Newswire, le 08/11/2010 : LONDRES, November 8, 2010 /PRNewswire/ -- Zebinix(R) (acétate d'eslicarbazépine) est un traitement anti-épileptique qui a été approuvé pour une utilisation limitée en Écosse à la suite d'une décision du Scottish Medicines Consortium (SMC)[1]. Conformément à cette nouvelle décision, Zebinix peut désormais être utilisé comme adjuvant chez les adultes présentant des crises épileptiques partielles, avec ou sans généralisation secondaire (lorsque les crises s'étendent aux deux côtés du cerveau). Le Comité ajoute que l'utilisation de Zebinix doit être limitée aux patients atteints d'épilepsie difficile à traiter (hautement réfractaire) qui ont précédemment suivi un traitement lourd et dont l'épilepsie demeure non maîtrisée par les anti-épileptiques actuels. […].
Les résulats de l'étude ATHENA avec l a dronédarone (Multaq(R)) discutés au Congrès Mondial de Cardiologie
PR Newswire, le 21/05/2008 : BUENOS AIRES, Argentine, May 21 /PRNewswire/ -- Aujourd'hui au World Congress of Cardiology (WCC), la conférence de presse intitulée 'Nouvelles perspectives de traitement de la fibrillation auriculaire' a soulignée que l'étude clinique ATHENA devrait changer la façon dont les cardiologues envisagent le traitement de la fibrillation auriculaire, l'arythmie cardiaque la plus commune. […].
La nouvelle formulation de Rebif(R) est approuvée dans l'Union Européenne
PR Newswire, le 30/08/2007 : GENÈVE, Suisse, August 30 /PRNewswire/ -- Merck Serono, une division de Merck KGaA, a annoncé aujourd'hui que la Commission Européenne a accordé une autorisation de mise sur le marché à sa nouvelle formulation de Rebif(R) (interféron bêta-1a), destinée au traitement de la sclérose en plaques de type récurrente. La nouvelle formulation de Rebif(R) a été développée dans le but d'optimiser le bénéfice thérapeutique en améliorant la tolérance à l'injection, tout en ciblant une amélioration du profil d'immunogénicité. Cette nouvelle formulation a été développée selon une approche innovante, basée sur des technologies de pointe. […].
Eisai annonce les résultats positifs de son étude de phase III portant sur l'action du Perampanel sur l'épilepsie partielle
PR Newswire, le 24/08/2010 : HATFIELD, Angleterre, August 24, 2010 /PRNewswire/ -- Eisai a aujourd'hui annoncé les résultats d'une étude de phase III portant sur le perampanel (E2007), premier composé expérimental d'une nouvelle classe de médicaments, antagoniste hautement sélectif et non compétitif des récepteurs du glutamate de type AMPA, découvert par Eisai et en cours de développement pour servir de traitement d'appoint destiné aux patients épileptiques souffrants de crises partielles. […].
Recommandation d'autorisation de Cyanokit(R) de Merck Serono en Europe
PR Newswire, le 24/09/2007 : GENEVE, Suisse, September 24 /PRNewswire/ -- Merck Serono, une division de Merck KGaA, a annoncé aujourd'hui que le Comité des Médicaments à Usage Humain (CHMP), le comité scientifique de l'Agence européenne pour l'évaluation des médicaments (EMEA), a émis un avis favorable pour Cyanokit(R) (substance active : hydroxocobalamine), son médicament pour le traitement de l'empoisonnement établi ou soupçonné au cyanure. A travers cet avis favorable, le Comité des Médicaments à Usage Humain recommande que la Commission européenne autorise la commercialisation de Cyanokit(R). […].