Vous êtes dans : Accueil > Actualités médicales >
Déficits immunitaires
14 résultats triés par date
affichage des articles n° 1 à 14
Déficits immunitaires : une nouvelle immunoglobuline humaine par voie sous-cutanée disponible en France, HYQVIA
SHIRE, le 12/01/2017 : Le laboratoire Shire annonce l’arrivée en France de sa nouvelle immunoglobuline humaine par voie sous-cutanée, HyQvia® 100 mg/ml, pour le traitement des déficits immunitaires primitifs et secondaires chez l'adulte, l'enfant et l'adolescent (âgé de 0 à 18 ans)1,2,3. […].
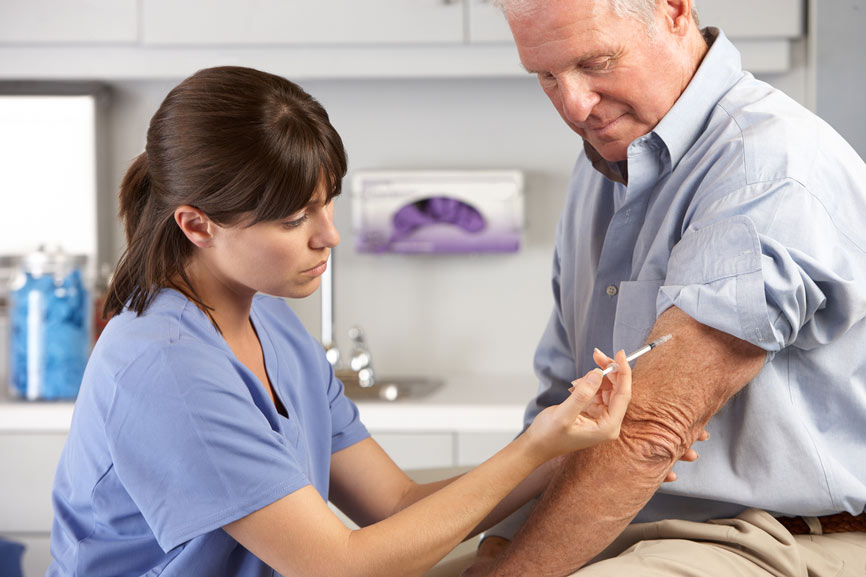
Grippe saisonnière : lancement de la campagne de vaccination
Caducee.net, le 17/10/2014 : C'est du 16 octobre au 31 janvier que l'assurance maladie invite plus de 10 millions de français à se faire vacciner contre la grippe.La stratégie vaccinale consiste à protéger les populations les plus vulnérables dans l'objectif de réduire le risque avéré de décès ou de complications graves en cas de grippe. […].
La grippe et les déficits immunitaires
CNAMTS, le 06/09/2004 : La grippe et le déficit immunitaire primitif graveChez les porteurs d’un déficit immunitaire, le système de défense de l’organisme a des capacités diminuées. Ils sont donc plus facilement sujets à des infections à répétition. Ces infections sont le plus souvent liées à des bactéries en cas de déficit de l’immunité humorale, et sont surtout virales en cas de déficit de l’immunité cellulaire. Ils sont donc plus exposés pour attraper la grippe. Mais chaque cas est particulier et la vaccination est à discuter avec le médecin. […].
Lancement des travaux de construction du nouveau centre de production d'IGIV de Grifols
PR Newswire, le 06/10/2008 : LOS ANGELES, October 7 /PRNewswire/ -- Grifols SA (Grifols), une société mondiale de soins de santé basée à Barcelone, Espagne, a inauguré aujourd'hui les travaux de construction d'un nouveau centre de production d'immunoglobulines intraveineuses (IGIV) de 92 000 pieds carrés situé dans son complexe de production de Los Angeles, Californie. Ce nouveau centre est la première étape du plan d'investissement à long terme de 600 millions USD annoncé en octobre 2007. L'objectif de ce plan est d'augmenter la production des traitements vitaux de coagulation, des immunoglobulines et de l'albumine de Grifols. Selon le calendrier des travaux et les exigences rigoureuses en matière d'autorisation réglementaire, le centre devrait pouvoir entreprendre ses activités de production de la nouvelle génération de produits d'IGIV de la société au début de 2013. […].
La teigne
C.Perbet, le 15/10/1999 : Le point complet sur la teigne : . […].
La teigne
C.Perbet, le 15/10/1999 : Le point complet sur la teigne : . […].
Prise en charge des maladies rares : Journée d’information au CHU Amiens-Picardie le 26 février 2016
Caducee.net, le 24/02/2016 : A l’occasion de la journée mondiale des maladies rares, une information est proposée aux professionnels de santé, aux familles concernées et au grand public le vendredi 26 février 2016 de 10h à 16h dans le hall du site sud du CHU Amiens-Picardie (nouveau bâtiment). Les professionnels du centre d’activité de génétique clinique et d’oncogénétique et du centre de référence maladies rares répondront aux questions sur les maladies avec anomalies du développement et/ou syndromes malformatifs. […].
LEUKOTAC obtient une ATU de cohorte dans le traitement de la maladie du greffon
ELSALYS, le 21/01/2020 : ElsaLys Biotech a annoncé le 9 janvier que l’ATUc a été accordée après évaluation, par l’ANSM et ses experts cliniques, d’un dossier comprenant des données sur la qualité, la sécurité et l’efficacité du médicament portant sur plusieurs centaines de patients inclus dans les essais cliniques ou traités par l’ATU nominative jusqu’en novembre 2015. Cette autorisation implique la mise en place d’un suivi renforcé (défini dans le PUT) des données d’efficacité et de sécurité obtenues chez les patients traités dans le cadre de cette ATUc. La prise en charge par inolimomab ne pourra être envisagée qu’en l’absence de possibilité d’inclusion du patient dans un essai clinique en cours. […].
L'Hôpital Foch inaugure la Clinique Universitaire des Bronches : un centre d'excellence pour les maladies bronchiques chroniques
Caducee.net, le 10/03/2025 : Face à la hausse des maladies respiratoires chroniques, l'Hôpital Foch ouvre la Clinique Universitaire des Bronches (CUB), un centre dédié aux soins, à la recherche et à la formation. Ce projet vise à améliorer le diagnostic, le traitement et la prévention des pathologies bronchiques, en intégrant des approches innovantes et des outils d'intelligence artificielle pour optimiser le suivi des patients. […].
Dépistage du col : la HAS rapproche les intervalles pour les femmes immunodéprimées
Caducee.net, le 12/10/2025 : La HAS publie des recommandations spécifiques pour le dépistage du cancer du col de l’utérus (CCU) chez les personnes immunodéprimées hors PVVIH. Cytologie annuelle de 25 à 29 ans, test HPV dès 30 ans puis tous les 3 ans si négatif, et décision individualisée après 65 ans : la cadence s’accélère pour répondre à un risque accru de persistance virale et de progression lésionnelle[1–2]. […].