Vous êtes dans : Accueil > Actualités médicales >
Corée
121 résultats triés par date
affichage des articles n° 73 à 90
NeoTract annonce la publication des résultats à cinq ans de son étude pivot portant sur le Système UroLift®
NeoTract, Inc., le 01/07/2017 : Dans la publication, les auteurs concluent que les résultats à cinq ans de l’étude démontrent que le Système UroLift « a atteint son niveau de maturité en tant que norme de soins pour l’HBP ». […].
L’Agence européenne des médicaments, débute l’examen des demandes d’autorisation de mise sur le marché de l’encorafenib et du binimetinib pour le traitement du mélanome avancé porteur d’une mutation BRAF
Pierre Fabre, le 28/08/2017 : « Les résultats de l’étude COLUMBUS, notamment pour ce qui concerne la survie sans progression, le taux de réponse objective, l’intensité de dose et la tolérance de l’association, fournissent un ensemble robuste et cohérent de données pour l’évaluation ». « Nous sommes ravis d’annoncer que l’EMA ait commencé l’examen du dossier d’autorisation de mise sur le marché de l’association binimetinib-encorafenib. En cas d’approbation, cette association développée en collaboration avec Array BioPharma pourrait représenter une nouvelle option de traitement importante pour les patients atteints de mélanome avancé et porteur d’une mutation BRAF » a déclaré Frédéric Duchesne, Directeur Général de Pierre Fabre Médicament et Santé. […].
Otsuka annonce les résultats de la phase III pour le Tolvaptan chez les patients atteints de polykystose rénale autosomique dominante (PKRAD)
Caducee.net, le 20/11/2017 : Otsuka Pharmaceutical Co., Ltd. (Otsuka) a annoncé les résultats détaillés de l’essai de phase III REPRISE évaluant l’efficacité et la tolérance du tolvaptan chez 1370 patients adultes atteints de polykystose rénale autosomique dominante (PKRAD) […].
L’UE suit les États-Unis et approuve l’inhibiteur de l’ALK « Alecensa® » de Chugai, en tant que traitement de première ligne pour le cancer bronchique non à petites cellules ALK-positif
Chugai Pharmaceutical Co., Ltd., le 22/12/2017 : « Suite à l’approbation du traitement de première ligne aux États-Unis en novembre 2017, c’est avec un grand plaisir que Chugai annonce l’approbation de l’Alecensa pour un traitement primaire dans l’UE. Une amélioration du pronostic est attendue chez les patients atteints de CBNPC avancé ALK-positif, qui reçoivent un traitement par l’Alecensa à un stade précoce », a déclaré le Dr Yasushi Ito, premier vice-président de Chugai, directeur de l’unité de gestion projet et cycle de vie. « Outre l’étude J-ALEX (JapicCTI-132316) menée au Japon, les résultats de l’étude ALEX (NCT02075840) menée à l’étranger ont également montré que ces nouvelles sont excellentes pour les patients. Nous sommes convaincus que l’Alecensa peut contribuer au traitement de nombreux patients dans le monde. » […].
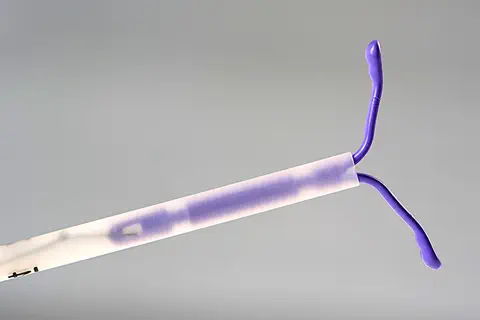
Kyleena, le nouveau système intra-utérin (SIU) de Bayer
BAYER, le 03/05/2018 : Bayer annonce aujourd’hui la mise à disposition de Kyleena® 19,5 mg, un nouveau système de diffusion intra-utérin (SIU) libérant une faible quantité totale de lévonorgestrel (LNG). Après une information éclairée sur les bénéfices et les risques, cette méthode contraceptive hormonale, réversible, de longue durée d’action, peut être proposée aux femmes n’y présentant pas de contre-indications quel que soit leur âge, qu’elles aient eu ou non des enfants, dans le respect des recommandations de l’HAS pour la prescription de contraception […].
Selon une étude clinique, la technologie SunLike de Seoul Semiconductor améliore la santé des yeux et la qualité du sommeil
Seoul Semiconductor Co., Ltd., le 19/07/2018 : Seoul Semiconductor Co., Ltd. (KOSDAQ : 046890), un leader mondial sur le marché de la conception et de la fabrication de diodes électroluminescentes (light emitting diodes, LED), a annoncé qu'une recherche avait montré que sa technologie « SunLike » offrait une LED optimisée pour l'éclairage centré sur l'homme et permettait d'améliorer la santé des yeux et la qualité du sommeil. […].
Pierre Fabre reçoit un avis positif du CHMP pour le BRAFTOVI® (encorafenib) MEKTOVI® (binimetinib) pour les patients adultes atteints d'un mélanome à mutation BRAF au stade avancé
Pierre Fabre, le 27/07/2018 : "Nous sommes très heureux de ce pas en avant qui nous rapproche de notre objectif: offrir le BRAFTOVI et le MEKTOVI aux patients européens atteints d'un mélanome à mutation BRAF au stade avancé," a déclaré Frédéric Duchesne, président et CEO de la division pharmaceutique de Pierre Fabre. "Si la Commission européenne approuve le BRAFTOVI et le MEKTOVI, ces patients, dont le pronostic actuel est peu favorable, disposeront d'une nouvelle option de traitement." […].
Foresee Pharmaceuticals annonce que le dernier patient a passé sa visite dans le cadre de l'étude de phase 3, avec 25 mg de LMIS (fp-001), pour traiter le cancer avancé de la prostate
Foresee Pharmaceuticals Co., Ltd., le 26/11/2018 : TAIPEI, Taïwan, 26 novembre 2018 /PRNewswire/ -- Foresee Pharmaceuticals Co., Ltd. (6576.TWO), a annoncé aujourd'hui que tous les patients ont finalisé l'essai multicentrique, multinational, de phase 3, du FP-001/LMIS (suspension injectable de leuprolide mésylate) de 25 mg, une formulation sous-cutanée de trois mois, prête à l'emploi, pour traiter le cancer avancé de la prostate. […].
Demande croissante en faveur de la solution de données de santé adaptée au RGPD fournie par Eventi Telematici et Penta Security Systems
Penta Security Systems Inc., le 20/12/2018 : Ce partenariat stratégique engendre une mise en œuvre croissante du logiciel de santé offrant une sécurité accrue dans les hôpitaux d'Europe. […].
Les données publiées dans The Lancet démontrent la non-infériorité du CT-P13 par rapport à l'infliximab de référence dans le traitement des maladies inflammatoires intestinales
Celltrion Healthcare, le 28/03/2019 : Le CT-P13 est déjà approuvé pour le traitement de huit maladies auto-immunes, notamment la MC, une forme de maladie inflammatoire intestinale (MII), dans plus de 80 pays, y compris les États-Unis, le Canada, le Japon et dans toute l'Europe. Il a été approuvé par l'EMA en 2013, et par la FDA en 2016. […].
Ostéoporose sévère : EVENITY® (romosozumab) reçoit le feu vert du CHMP
AMGEN, le 19/10/2019 : UCB et Amgen ont annoncé aujourd'hui qu'à l'issue d'une procédure d’un nouvel examen, le comité des médicaments à usage humain (CHMP) de l'Agence européenne des médicaments (EMA) a émis un avis favorable pour l'autorisation de mise sur le marché d’EVENITY® (romosozumab) dans le traitement de l'ostéoporose sévère chez les femmes ménopausées présentant un risque élevé de fracture et n'ayant pas d'antécédents d'infarctus du myocarde ou d'accident vasculaire cérébral. Le romosozumab est un nouvel anticorps monoclonal à double mode d’action, qui principalement augmente la formation osseuse et, dans une moindre mesure, réduit la résorption osseuse (ou perte osseuse). […].
#Coronavirus 2019 : Repérer et prendre en charge un patient suspect
Caducee.net, le 27/01/2020 : La direction générale de la Santé met à la disposition des professionnels de santé et particulièrement des médecins de premier recours des fiches pratiques sur la conduite à tenir en cas de suspicion d’infection à nouveau coronavirus 2019. […].
#COVID19 : Un médecin américain aurait traité avec succès plus de 500 patients avec l’hydroxychloroquine
Caducee.net, le 26/03/2020 : Le Dr Zev Zelenko est un médecin qui exerce à Monroe dans l’état de New York, l’un des états américains les plus touchés par COVID-19, selon l’OMS. Il vient d’écrire une lettre ouverte à l’attention du président Trump et des médecins du monde entier dans le but de partager les succès qu’il aurait obtenus en traitant 500 patients à risques présentant les symptômes du COVID-19. Cette lettre a été reprise par différents média américains. Nous vous en livrons une traduction aussi fidèle que possible mais attirons votre attention sur le fait que les informations qu’elle contient doivent être prises en compte avec toutes les précautions qui s’imposent. […].
#COVID19 : un syndicat de médecins poursuit l’État en référé pour la généralisation du dépistage et du traitement à la #chloroquine du Pr Raoult
Caducee.net, le 28/03/2020 : Le syndicat des médecins d’Aix et région (SMAER) en a assez. « Assez des contradictions, des mensonges d’État » et de son incapacité à protéger les soignants et les patients. Il poursuit donc l’État en référé afin d’obtenir des masques FFP2 ainsi que la généralisation du dépistage et du traitement préconisé par le Pr Raoult. Le recours a été déposé mercredi devant le Conseil d’État et a été plaidé jeudi. […].
Prévention du #COVID19 : faut-il porter un masque dans la rue ?
Caducee.net, le 01/04/2020 : Alors qu’en France le port de masque n’est pas indiqué en population générale, des scientifiques de renom expliquent qu’il s’agit d’une grosse erreur de prévention face aux risques de transmission du coronavirus. […].
#COVID19 : L’académie de Médecine propose de rendre obligatoire le port de masques antiprojection « alternatifs » pour le public
Académie de Médecine, le 03/04/2020 : Tirant les leçons de l'expérience de certains pays asiatiques face au covid-19, l’académie de Médecine recommande dorénavant de rendre obligatoire le port de masques « faits maison » pour le public lors des sorties pendant la période de confinement et même au-delà lors de la levée du confinement. Elle rappelle néanmoins que les masques FFP2 et chirurgicaux doivent en priorité être attribués aux établissements de santé et à la médecine de ville. […].
Stallergenes greer dépose une demande d’AMM pour son comprimé sublingual d’immunothérapie allergénique aux acariens
Businesswire, le 04/05/2020 : Stallergenes Greer, laboratoire biopharmaceutique spécialisé dans le traitement des allergies respiratoires, annonce le dépôt d’une demande d’autorisation de mise sur le marché (AMM) pour son comprimé d’immunothérapie sublinguale STAGR320, dans le cadre d’une procédure européenne décentralisée. […].
Merck obtient des brevets américains pour sa technologie fondamentale CRISPR-Cas9
Merck, le 11/05/2020 : DARMSTADT, Allemagne, 11 mai 2020 /PRNewswire/ -- Merck, une société scientifique et technologique de premier plan, a annoncé aujourd'hui que deux de ses brevets d'édition génomique assistée par CRISPR-Cas9 ont été acceptés aux États-Unis. Cela permet ainsi à Merck de soutenir les scientifiques et chercheurs américains dans leurs travaux pour faire avancer et protéger les programmes de développement de thérapies géniques. La société négocie actuellement la concession sous licence de sa technologie fondamentale à des fins thérapeutiques et autres, et recherche des partenaires de collaboration pour la recherche et le développement de produits. […].