Vous êtes dans : Accueil > Actualités médicales >
Ongles
20 résultats triés par date
affichage des articles n° 1 à 18
Psoriasis : une maladie cutanée qui déborde largement la peau
Caducee.net, le 15/02/2026 : Longtemps perçu comme une affection dermatologique avant tout visible, le psoriasis impose en réalité une lecture plus large, à la fois inflammatoire, chronique et systémique. En France, la maladie concerne entre 2 et 3 % de la population et débute le plus souvent entre 20 et 40 ans, avec des formes parfois précoces, parfois articulaires, parfois sévères, toujours marquées par une évolution en poussées et un retentissement clinique qui dépasse la seule lésion cutanée.[1] […].
Psoriasis : une maladie cutanée qui déborde largement la peau
Caducee.net, le 15/02/2026 : Longtemps perçu comme une affection dermatologique avant tout visible, le psoriasis impose en réalité une lecture plus large, à la fois inflammatoire, chronique et systémique. En France, la maladie concerne entre 2 et 3 % de la population et débute le plus souvent entre 20 et 40 ans, avec des formes parfois précoces, parfois articulaires, parfois sévères, toujours marquées par une évolution en poussées et un retentissement clinique qui dépasse la seule lésion cutanée.[1] […].
Le mercure contenu dans les poissons augmenterait le risque coronarien
Caducee.net, le 28/11/2002 : Deux études publiées aujourd’hui dans le New England Journal of Medicine posent la question de la toxicité du mercure comme facteur de risque coronarien. La première étude suggère que le mercure contenu dans certains poissons augmente le risque coronarien tandis que la deuxième ne retrouve pas cette relation, sans pour autant en écarter définitivement la possibilité. […].
Nestlé Skin Health créera un réseau de centres d'innovation consacré à la promotion de la santé dermatologique
Nestlé Skin Health, le 11/12/2014 : Humberto C. Antunes, Nestle Skin Health CEO (Photo: Business Wire) […].
Des bains de pieds responsables de furonculoses…
Caducee.net, le 06/05/2002 : Un manque de mesures de désinfection dans un salon de beauté californien spécialisé dans les soins pédicures est à l'origine de plus d'une centaine de cas de furonculose à mycobactéries. Une contamination d'un système hydraulique est en cause. […].
Les professionnels de santé appellent au vote d’une loi « Booba » pour endiguer la désinformation médicale
Caducee.net, le 30/01/2024 : Face à la montée de la désinformation médicale, des dizaines de personnalités et d’institutions médicales lancent un appel dans une tribune publiée par l’Express à renforcer le cadre législatif pour lutter contre les « fakenews » médicales et promouvoir des informations basées sur des preuves scientifiques. […].
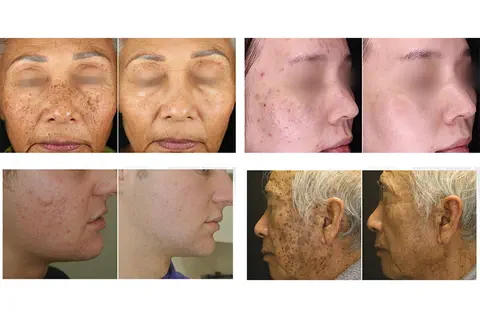
Cynosure lance PicoSure® Pro à l'AMWC : le premier et le seul laser de 755 nm au monde approuvé par la FDA pour traiter la pigmentation du mélasma
PRNEWSWIRE, le 01/04/2022 : CHISWICK, Angleterre, 1er avril 2022 /PRNewswire/ -- Cynosure lancera le système PicoSure® Pro lors du congrès de l'AMWC à Monaco ce week-end et organisera un symposium de lancement autonome, dirigé par le Dr Christine Dierickx, experte internationale de renom, qui présentera cette dernière amélioration du meilleur système PicoSure de sa catégorie. PicoSure® Pro est le premier et le seul laser picoseconde de 755 nm approuvé par la FDA sur le marché, et fournit de l'énergie de manière unique en un milliardième de seconde, en utilisant la pression au lieu de la chaleur pour fournir des traitements sûrs et efficaces contre la pigmentation indésirable et la revitalisation de la peau pour tous les types de peau. […].
Covid-19 et suivi des patients positifs en ambulatoire : la HAS actualise ses recommandations
Caducee.net, le 20/04/2021 : La Haute Autorité de Santé a publié sur un son site Internet un document précisant, sous forme de réponses rapides, la conduite à tenir en médecine de ville face à un cas confirmé d’infection par le SARS-COV-2. Ces nouvelles recommandations s’adressent non seulement aux médecins généralistes, mais aussi à tous les professionnels de santé qui peuvent être amenés à communiquer à un patient un test de diagnostic positif notamment les infirmiers, les pharmaciens d’officine et biologistes médicaux. […].
Médicaments remboursables : une étude de l’Assurance Maladie pour comprendre les principales évolutions de l’année 2003
CNAM , le 20/09/2004 : Au cours de l’année 2003, les différents régimes d’Assurance Maladie ont remboursé plus de 2,6 milliards de boîtes, flacons, ou autres présentations de médicaments acquises dans les 23000 pharmacies d’officines pour un montant total de 16,5 milliards d’euros ( 4,6% par rapport à 2002). […].
Premier lien établi entre la télomérase et une maladie génétique
Caducee.net, le 02/12/1999 : Des chercheurs américains viennent pour la première fois d’établir un lien entre un mauvais fonctionnement de la télomérase, enzyme qui protège les fragiles extrémités des chromosomes (télomères) lors des divisions cellulaires, et une maladie génétique. […].
Galderma annonce l'autorisation du gel Differin(R) 0,1 % au Japon
PR Newswire, le 17/07/2008 : LAUSANNE, Suisse, July 17 /PRNewswire/ -- Galderma Pharma S.A., société pharmaceutique internationale spécialisée en dermatologie, a annoncé aujourd'hui que le ministère de la santé, du travail et du bien-être du Japon a autorisé la commercialisation du gel Differin(R) 0,1 % (adapalène), un nouveau traitement topique de l'acné, au Japon. Le médicament sera commercialisé au Japon par l'intermédiaire de Galderma KK, la filiale japonaise en propriété exclusive de Galderma, et de son partenaire stratégique Shionogi. […].
HUMIRA(R) d'Abbott reçoit un avis positif de l'EMEA pour le traitement du psoriasis en plaques modéré à sévère
PR Newswire, le 16/11/2007 : ABBOTT PARK, Illinois, November 17 /PRNewswire/ -- Le Comité des produits médicinaux à usage humain (CPMUH), le comité scientifique de l'Agence européenne du Médicament (EMEA), a accordé à Abbott (NYSE : ABT) un avis positif par lequel il recommande l'approbation d'HUMIRA(R) (adalimumab) pour le traitement du psoriasis en plaques d'intensité modérée à sévère. Le psoriasis constituera la cinquième indication pour laquelle HUMIRA est approuvé. […].
HUMIRA(R) d'Abbott est autorisé dans l'Union Européenne pour le traitement du psoriasis en plaques modéré à sévère
PR Newswire, le 21/12/2007 : ABBOTT PARK, Illinois, December 21 /PRNewswire/ -- Abbott (NYSE: ABT) a obtenu de la Commission européenne l'autorisation de commercialisation pour l'utilisation d'HUMIRA(R)(adalimumab) en guise de traitement du psoriasis en plaques modéré à sévère. HUMIRA est le premier produit biologique totalement humain auto-injectable pour le traitement du psoriasis. Dans un essai clinique, plus de 80 % des patients sous HUMIRA ont présenté une amélioration de la peau d'au moins 75 %, tandis que dans un autre essai, près des trois quarts des patients ont obtenu une amélioration de 75 %. Dans les deux essais, près de la moitié des patients sous HUMIRA ont présenté une amélioration de la peau de 90 % après seulement 16 semaines de traitement. Le psoriasis est la cinquième indication d'HUMIRA dans l'Union Européenne. Une autorisation réglementaire d'HUMIRA pour le traitement du psoriasis est aussi examinée par la Food and Drug Administration des Etats-Unis. […].
Galderma conclut son offre publique d'achat de CollaGenex
PR Newswire, le 07/04/2008 : LAUSANNE, Suisse, April 7 /PRNewswire/ -- Galderma Pharma S.A., société pharmaceutique internationale spécialisée qui se concentre sur les soins dermatologiques, a annoncé aujourd'hui que sa société de portefeuille américaine, Galderma Laboratories, Inc., a conclu son offre publique d'achat au comptant pour CollaGenex Pharmaceuticals, Inc. (Nasdaq : CGPI). L'offre s'est close le vendredi 4 avril 2008 à minuit, heure de New York. […].
L’arsenic perturbe le système de réparation de l’ADN
Caducee.net, le 07/04/2003 : L’exposition à l’arsenic dans l’eau de boisson est associée à une augmentation des risques de cancer. Les mécanismes biologiques impliqués sont encore mal connus mais il semble que l’arsenic perturbe le système de réparation de l’ADN et favorise ainsi l’apparition des cancers. […].
La création du premier singe transgénique pose la question des applications de cette technique
Caducee.net, le 12/01/2001 : Des scientifiques décrivent dans la revue Science la création du premier primate non humain génétiquement modifié par insertion dans son génome du gène codant la GFP (green fluorescent protein). Cette technique constitue une avancée notable pour la mise au point de nouveau modèles animaux plus proches de l'homme que ne le sont les rongeurs souvent employés dans la recherche médicale. Néanmoins, le transfert de cette technologie à l'homme paraît encore lointain. […].
Un essai randomisé sur l’utilisation de la toxine botulique dans le traitement de la spasticité musculaire des membres supérieurs après un AVC
Caducee.net, le 09/10/2000 : Le Dysport (toxine botulique de type A) permet de réduire les douleurs et la spasticité musculaire des membres supérieurs consécutives à un AVC. Un essai randomisé en double aveugle avec contrôle placebo, publié dans la revue Stroke, a évalué l’efficacité de 3 doses de Dysport. […].