Sanofi : Sanofi et MannKind annoncent la mise à disposition d'Afrezza®, la seule insuline à inhaler, aux États-Unis
Paris et Valencia (Californie) - Le 3 février 2015 - Sanofi et MannKind Corporation annoncent aujourd'hui qu'Afrezza ® (insuline humaine), poudre à inhaler, la seule insuline à inhaler, est désormais disponible sur ordonnance dans les officines de l'ensemble du territoire des États-Unis. Afrezza est approuvé par la Food and Drug Administration des États-Unis pour le contrôle de l'hyperglycémie des adultes atteints de diabète de type1 et de type2.
«De nombreuses personnes vivant avec le diabète ne parviennent pas à contrôler leur glycémie malgré les médicaments qu'elles prennent et pourraient bénéficier d'un traitement par insuline. Aujourd'hui, elles ont à leur disposition une nouvelle option pour s'administrer de l'insuline autrement que par injection» , a déclaré le DrJanet McGill, Professeur de médecine à la Faculté de médecine de l'Université Washington de St. Louis et investigateur des essais cliniques consacrés à Afrezza. «Cette option d'administration pourrait modifier le dialogue entre les professionnels de santé et les personnes atteintes de diabète quant à l'instauration d'une insulinothérapie ou son intensification.»
Afrezza peut permettre de contrôler l'hyperglycémie dans le cadre d'une prise en charge du diabète pouvant inclure un régime alimentaire, un programme d'exercice physique et d'autres antidiabétiques. Afrezza ne doit pas être prescrit aux patients présentant une maladie respiratoire chronique telle que l'asthme ou la BPCO. Afrezza ne peut non plus être utilisé dans le traitement de l'acidocétose diabétique. Afrezza est déconseillé aux fumeurs ou aux patients qui viennent d'arrêter de fumer.
«Afrezza est un ajout important au portefeuille en pleine expansion de Sanofi dans le diabète. Ce portefeuille comporte des offres intégrées et personnalisées et témoigne de notre volonté de mettre des thérapies innovantes à la disposition des personnes souffrant de cette maladie» , a déclaré Pierre Chancel, Senior Vice-Président, Division Diabète de Sanofi. «Le besoin d'une insuline qu'il est possible de s'administrer autrement que par injection est indéniable et notre Groupe s'engage à mettre cette nouvelle option thérapeutique à la disposition des patients.»
«Nous sommes extrêmement fiers de voir l'aboutissement des nombreuses années de travail consacrées au développement d'Afrezza et sa mise à disposition aux patients pour les aider à prendre en charge leur diabète» , a déclaré Alfred Mann, Président Exécutif de MannKind Corporation.
A propos d'Afrezza
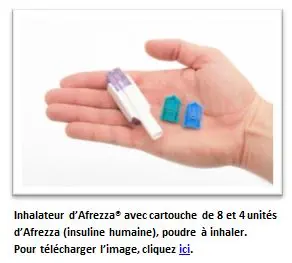
Afrezza est une insuline à inhaler d'action rapide indiquée pour améliorer le contrôle de la glycémie chez l'adulte atteint de diabète de type 1 ou de type 2. Le produit consiste en une formulation sèche d'insuline humaine diffusée par un petit inhalateur portatif. Administré au début du repas, Afrezza pénètre profondément dans les poumons où il se dissout immédiatement et l'insuline passe rapidement dans la circulation sanguine. Les taux d'insuline atteignent leur pic en 12 à 15 minutes. Afrezza est disponible en cartouches de 4 et 8unités de poudre d'insuline et peut être utilisé, conformément aux prescriptions d'un professionnel de santé, en association avec d'autres antidiabétiques pour atteindre le taux cible de glycémie. Pour les doses d'Afrezza supérieures à 8unités, les patients peuvent utiliser une combinaison de cartouches de 4 et de 8unités. D'autres formats de cartouche sont envisagés. L'inhalateur jetable peut être utilisé pendant une durée maximale de 15jours; il doit être conservé au sec et au propre, son embout muni du capuchon protecteur. Il peut au besoin être nettoyé avec un chiffon propre et sec.
Sanofi et MannKind ont conclu un accord de licence exclusif mondial pour développer et commercialiser Afrezza. En vertu de cet accord, Sanofi est chargé, à l'échelle mondiale, des activités commerciales, des affaires réglementaires et du développement du produit.
A propos de Sanofi Diabète
Sanofi s'engage à aider les patients à prendre en charge cette maladie complexe qu'est le diabète, en leur proposant des solutions innovantes, intégrées et personnalisées. Grâce à une écoute attentive des patients diabétiques et à son engagement à leurs côtés, le Groupe a formé plusieurs partenariats dans le but de développer des outils diagnostiques, des traitements, des services et des dispositifs médicaux, notamment des lecteurs de glycémie innovants. Sanofi commercialise des médicaments injectables et oraux pour le traitement du diabète de type 1 et de type 2.
A propos de Sanofi
Sanofi, un leader mondial de la santé, recherche, développe et commercialise des solutions thérapeutiques centrées sur les besoins des patients. Sanofi possède des atouts fondamentaux dans le domaine de la santé avec sept plateformes de croissance : la prise en charge du diabète, les vaccins humains, les produits innovants, la santé grand public, les marchés émergents, la santé animale et le nouveau Genzyme. Sanofi est coté à Paris (EURONEXT : SAN ) et à New York (NYSE : SNY ).
A propos de MannKind Corporation
MannKind Corporation (Nasdaq : MNKD ) est une entreprise spécialisée dans la découverte, le développement et la commercialisation de traitements pour les patients atteints de maladies telles que le diabète. MannKind possède un site internet (www.mannkindcorp.com) sur lequel sont régulièrement affichés ses communiqués de presse et les informations sur la société. Les personnes intéressées peuvent s'inscrire sur le site de MannKind pour recevoir des alertes envoyées automatiquement par courrier électronique quand MannKind émet des communiqués de presse, dépose un rapport auprès des Commissions des Opérations de Bourse ou affiche d'autres informations sur son site.
Déclarations prospectives
Ce communiqué contient des déclarations prospectives telles que définies dans le « Private Securities Litigation Reform Act » de 1995. Ces déclarations ne constituent pas des faits historiques. Ces déclarations comprennent des projections et des estimations ainsi que les hypothèses sur lesquelles celles-ci reposent, des déclarations portant sur des projets, des objectifs, des intentions et des attentes concernant des résultats financiers, des événements, des opérations, des services futurs, le développement de produits et leur potentiel ou les performances futures. Ces déclarations prospectives peuvent souvent être identifiées par les mots « s'attendre à », « anticiper », « croire », « avoir l'intention de », « estimer » ou « planifier », ainsi que par d'autres termes similaires. Bien que la direction de Sanofi estime que ces déclarations prospectives sont raisonnables, les investisseurs sont alertés sur le fait que ces déclarations prospectives sont soumises à de nombreux risques et incertitudes, difficilement prévisibles et généralement en dehors du contrôle de Sanofi, qui peuvent impliquer que les résultats et événements effectifs réalisés diffèrent significativement de ceux qui sont exprimés, induits ou prévus dans les informations et déclarations prospectives. Ces risques et incertitudes comprennent notamment les incertitudes inhérentes à la recherche et développement, les futures données cliniques et analyses, y compris postérieures à la mise sur le marché, les décisions des autorités réglementaires, telles que la FDA ou l'EMA, d'approbation ou non, et à quelle date, de la demande de dépôt d'un médicament, d'un procédé ou d'un produit biologique pour l'un de ces produits candidats, ainsi que leurs décisions relatives à l'étiquetage et d'autres facteurs qui peuvent affecter la disponibilité ou le potentiel commercial de ces produits candidats, l'absence de garantie que les produits candidats s'ils sont approuvés seront un succès commercial, l'approbation future et le succès commercial d'alternatives thérapeutiques, la capacité du Groupe à saisir des opportunités de croissance externe, l'évolution des cours de change et des taux d'intérêt, l'impact de la politique de maîtrise des coûts opérationnels et leur évolution, le nombre moyens d'actions en circulation ainsi que ceux qui sont développés ou identifiés dans les documents publics déposés par Sanofi auprès de l'AMF et de la SEC, y compris ceux énumérés dans les rubriques « Facteurs de risque » et « Déclarations prospectives » du document de référence 2013 de Sanofi, qui a été déposé auprès de l'AMF ainsi que dans les rubriques « Risk Factors » et « Cautionary Statement Concerning Forward-Looking Statements » du rapport annuel 2013 sur Form 20-F de Sanofi, qui a été déposé auprès de la SEC. Sanofi ne prend aucun engagement de mettre à jour les informations et déclarations prospectives sous réserve de la réglementation applicable notamment les articles 223-1 et suivants du règlement général de l'Autorité des marchés financiers .
Conflit d'intérêts: Après avoir participé à des essais cliniques d'Afrezza, le Dr Janet McGill a été consultante auprès de MannKind Corporation et de Sanofi en 2014. Elle est actuellement consultante pour Sanofi.
Afrezza ® est une marque déposée de MannKind Corporation.
Brevet: voir http://www.mannkindcorp.com/our-technology-patent-notices.htm
| Fabriqué par: MannKind Corporation Danbury, Connecticut 06810 |
Distribué par: Sanofi-aventis U.S. LLC Bridgewater, New Jersey 08807 UNE ENTREPRISE DU GROUPE SANOFI |
Contacts:
| Sanofi Relations Presse | Sanofi Relations Investisseurs | MannKind Relations Investisseurs |
| Jack Cox | Sébastien Martel | Matthew Pfeffer |
| Tél.: 33 (0) 1 53 77 46 46 | Tél.: 33 (0) 1 53 77 45 45 | 1-661-775-5300 |
| jack.cox@sanofi.com | ir@sanofi.com | mpfeffer@mannkindcorp.com |
| CommunicationSanofiUS Diabetes Susan Brooks 1 908 981 6566 susan.brooks@sanofi.com |
Communication Sanofi Diabète Global Phil McNamara 1 908 981 5497 philip.mcnamara@sanofi.com |
The issuer of this announcement warrants that they are solely responsible for the content, accuracy and originality of the information contained therein.
Source: Sanofi via GlobeNewswire
Descripteur MESH : Insuline , Diabète , Hyperglycémie , Patients , Californie , Santé , Glycémie , Personnes , Solutions , Recherche , Repas , Essais , Maladie , Diabète de type 1 , Croissance , Médecine , Physique , Maîtrise des coûts , Paris , Politique , Régime alimentaire , Risque , Thérapeutique , Travail , Vaccins , Washington , Objectifs , New York , New Jersey , Acidocétose diabétique , Internet , Intention , Facteurs de risque , Exercice physique , Électronique , Courrier électronique , Connecticut , Circulation sanguine , Asthme , Association , Adulte

