Pour une prise en charge personnalisée du patient hémophile, Shire lance l’application myPKiT
Hémophilie A : la plus fréquente des hémophilies1
L’hémophilie A est une affection héréditaire familiale autosomique récessive, liée au chromosome X, caractérisée par un déficit du facteur de coagulation VIII (FVIII). Elle est la plus fréquente des hémophilies et s’observe essentiellement chez les garçons. Les filles peuvent en être atteintes uniquement dans le rare cas où leur père est hémophile et leur mère porteuse du gène, ou dans les cas d’inactivation du chromosome X normal, c’est-à-dire non porteur du gène muté.
Selon la nature de la mutation génétique qui est à l’origine de la maladie, le facteur de coagulation peut être totalement absent, ou présent, mais sous une forme dysfonctionnelle (taux de FVIII très, modérément ou peu diminué).
Épidémiologie
L’hémophilie A représente 60 % des maladies hémorragiques en rapport avec un déficit héréditaire d’une protéine coagulante. Plus concrètement, elle concerne 5 762 cas sur 9 543 patients suivis dans les Centres de traitement de l’hémophilie (CTH) du réseau FranceCoag2. Sur ces 5 762 patients atteints
d’hémophilie A répertoriés en France, 1 849 — soit environ un tiers — présentent une hémophilie sévère (définie par un taux de FVIII de moins de 1 %) tandis que 808 autres ont une hémophilie considérée comme modérée et 3 105 une hémophilie mineure.
Symptômes, complications
En raison du manque de FVIII, les patients hémophiles A sont exposés au risque de présenter des hémorragies, potentiellement graves. Le degré de sévérité des manifestations cliniques de la maladie varient en fonction de la sévérité du déficit en facteurs de coagulation :
• si l’hémophilie est sévère, elle se manifeste par des hémorragies spontanées fréquentes et des saignements anormaux (à la suite de blessures mineures, d’une chirurgie ou d’une extraction dentaire),
• si la maladie est modérée, elle provoque des saignements anormaux, mais les hémorragies spontanées sont rares,
• si elle est mineure, elle entraîne des saignements anormaux, mais pas d’hémorragie spontanée.
« Les hémorragies spontanées qui surviennent lorsque le déficit en facteur VIII est sévère sont principalement des hémorragies intra-articulaires ou hémarthroses, qui représentent 80 % des accidents hémorragiques », précise le Dr Thierry Lambert, Centre de Référence pour le Traitement des maladies Hémorragiques (CRTH), Hôpital Bicêtre AP-HP, Paris. S’ils se répètent, les saignements intra — articulaires exposent au risque d’altération de l’articulation puis de dégradation importante de la fonction articulaire (arthropathie hémophilique). Risque majeur de la destruction articulaire : la perte de mobilité, le handicap et la détérioration de la qualité de vie. « L’enjeu majeur des traitements est d’amener les hémophiles à l’âge adulte dans un bon état articulaire, pour qu’ils puissent avoir une vie la plus normale possible », déclare le Dr Thierry Lambert.
Traitements
Les traitements anti-hémophiliques permettent, pendant un laps de temps limité, d’avoir une coagulation normale en apportant le facteur de coagulation manquant. Ils permettent ainsi de limiter le risque de saignement ou de traiter un saignement. Ils sont administrés dans deux circonstances :
– à la demande, en cas d’accident hémorragique : le traitement doit débuter le plus tôt possible après la survenue de l’accident pour traiter l’hémorragie et prévenir les séquelles,
– en préventif, pour prévenir le risque de saignements, réduire leur fréquence ainsi que les séquelles invalidantes qu’ils peuvent induire, diminuer l’absentéisme (scolaire ou professionnel), assurer une meilleure qualité de vie. Le traitement préventif consiste à réaliser des injections régulières et systématiques de concentrés de FVIII.
Les produits anti-hémophiliques sont administrés par voie IV à l’hôpital ou à domicile par une infirmière ou un médecin. Le traitement à domicile est recommandé pour favoriser l’autonomie et une meilleure qualité de vie. L’injection est alors réalisée par une infirmière libérale, par un médecin, par un proche ou par l’hémophile lui-même (lors d’un accident hémorragique ou en prophylaxie). Des stages d’apprentissage pour l’auto-traitement sont organisés pour les parents et les enfants, par les CTH et par l’Association Française des Hémophiles.
En parallèle au traitement, un certain nombre de précautions sont à prendre pour éviter autant que possible les accidents hémorragiques : proscrire les injections intramusculaires, les sports qui comportent un risque de choc, etc.
Les enjeux de la prise en charge des patients atteints d’hémophilie A
La prophylaxie recommandée pour une prise en charge optimale
Un traitement prophylactique par FVIII est préconisé par la Fédération mondiale de l’hémophilie, pour une prise en charge optimale de l’hémophilie A sévère. Il vise à réduire le nombre d’épisodes hémorragiques dont les saignements articulaires, à améliorer la qualité de vie des patients. « Un taux de facteur de coagulation quasiment nul a été identifié comme facteur de risque d’atteinte articulaire dans les hémophilies sévères. La seule façon d’éviter que s’installent ces dégâts articulaires est le traitement prophylactique, qui consiste à programmer des injections répétées du facteur VIII manquant », rapporte le Dr Thierry Lambert.
Les facteurs de coagulation ayant une durée de vie courte, de l’ordre de quelques heures, un rythme d’injections pluri-hebdomadaire est nécessaire pour maintenir la prévention des accidents et donc des dégâts articulaires (deux ou trois fois par semaine). Leur administration doit, en outre, débuter tôt, vers l’âge de 2 ans, dès que l’enfant commence à marcher, avant que les premiers saignements intra — articulaires surviennent. « Avec ce rythme d’administration, on arrive à prévenir la grande majorité des accidents spontanés hémorragiques, mais cela implique des contraintes lourdes : pluri-injections par voie IV, chez les enfants jeunes », souligne le Dr Thierry Lambert. « Toute l’action des centres d’hémophilie consiste à accompagner les patients et leurs familles pour rendre le traitement acceptable, à les aider à en comprendre les enjeux ». L’observance du traitement, le bon suivi des injections jouent en effet un rôle capital dans l’efficacité du traitement prophylactique.
L’intérêt d’une prophylaxie personnalisée
L’enjeu actuel des traitements est de préserver le plus tôt possible les articulations des patients hémophiles, particulièrement atteintes lors de saignements répétés. Afin de préserver le capital articulaire, un objectif « zéro saignement » est visé. Cependant cet objectif ne peut être imaginé que si chaque traitement est personnalisé, car chaque patient hémophile est unique. En d’autres termes, le traitement prophylactique doit être adapté à chaque patient, en tenant compte de son âge, de son phénotype hémorragique, de son mode de vie (personnelle, professionnelle), de son niveau d’activité physique, mais aussi de ses paramètres pharmacocinétiques. « Un traitement prophylactique bien conduit et adapté aux caractéristiques du patient, au mode de vie, à la réaction individuelle, permet d’arriver au mieux à l’objectif qui est d’éviter les dégâts articulaires. L’important est d’adapter le rythme du traitement à la vie du patient et non l’inverse », insiste le Dr Thierry Lambert.
L’adaptation du traitement à la vie du patient doit notamment prendre en compte l’activité physique de celui-ci. « En cas de pratique sportive, il est essentiel de faire correspondre les moments où la couverture hémostatique est la meilleure, lorsque le taux de facteur VIII est suffisant, soit dans les heures qui suivent l’injection, avec les moments d’activités », signale le Dr Thierry Lambert.
L’importance de l’évaluation des paramètres pharmacocinétiques
La réponse pharmacocinétique à l’administration de FVIII étant variable d’un patient à un autre (le taux auquel monte le facteur lorsqu’on l’injecte et sa rapidité de diminution peut varier d’une personne à l’autre), l’évaluation des paramètres pharmacocinétiques (demi-vie, aire sous la courbe) représente l’un des facteurs les plus importants pour adapter et personnaliser le traitement prophylactique. La demi-vie du facteur VIII peut en effet fluctuer de 6 à 25 heures. Puisque chaque patient élimine le facteur de coagulation de manière différente, la quantité de FVIII donnée en prophylaxie doit être adaptée à ses besoins.
Par ailleurs, il a été montré que le risque d’hémorragies totales et d’hémarthroses s’accroît avec le temps durant lequel le taux de facteur VIII s’abaisse en dessous de 1 %. Toutefois, un taux unique de facteur VIII à 1 % ne suffit pas pour limiter les saignements. Ainsi, certains patients sous prophylaxie et qui visent un taux minimal ≥ 1 % souffrent toujours de saignements et des taux de FVIII > 3 % sont parfois nécessaires pour les éviter (par exemple, si le patient a déjà une articulation abîmée). D’où l’intérêt d’adapter le taux cible minimal de FVIII optimal (permettant de prévenir les saignements) au profil, à la situation clinique et au mode de vie de chaque patient.
Pour une personnalisation optimale du traitement (la bonne dose au bon moment, adaptée au patient), il est donc essentiel de prendre en compte les paramètres pharmacocinétiques individuels et d’adapter les taux cibles aux activités de chaque patient.
Objectif « zéro saignement » : le dispositif médical myPKFiT® pour les professionnels de santé
Shire, un acteur engagé
Acteur majeur et expert reconnu de l’hémophilie, Shire a évolué au fil du temps en termes de prise en charge des patients, passant de la mise à disposition d’un traitement à la demande à celle d’un traitement prophylactique, systématiquement proposé chez les jeunes, dans le but de préserver les articulations, en essayant d’éviter tous les saignements. « C’est donc une tolérance “zéro” que nous prônons, pour essayer d’atteindre “zéro saignements”, y compris les micro-saignements qui peuvent avoir à terme un impact négatif sur les articulations des patients », déclare le Dr Jean Delonca, directeur médical chez Shire France. Or la personnalisation du traitement adaptée à la clinique du patient, à son mode de vie, à son histoire, à ses besoins et à son activité est le seul moyen d’atteindre l’objectif « zéro saignement ».
« Chez Shire, nous mettons à disposition des patients des innovations thérapeutiques tout en améliorant leur prise en charge et leur qualité de vie, notamment en apportant des services qui peuvent aider et faciliter la vie des patients et de leurs familles. Nous avons ainsi développé deux outils complémentaires : le logiciel myPKFiT destiné aux professionnels de santé, qui permet d’estimer la pharmacocinétique chez un patient donné et qui contribue à une prophylaxie personnalisée, et l’application myPKFiT pour les patients », signale le Dr Jean Delonca.
myPKFiT : un outil de personnalisation du traitement et d’optimisation thérapeutique
Pour accompagner, vers cet objectif « zéro saignement », les professionnels de santé impliqués dans le parcours de soins des patients hémophiles, le laboratoire Shire a mis à leur disposition en 2016 un logiciel en ligne : myPKFiT.
Ce dispositif médical CE a été conçu pour personnaliser le traitement avec ADVATE. Il permet de définir le profil pharmacocinétique de chaque patient et, de ce fait, d’ajuster les doses de FVIII, de déterminer la fréquence des injections pour atteindre un taux cible prédéfini (1 %, 2 %, 3 %...). Ceci afin d’obtenir l’objectif de couverture hémostatique espéré, de prévenir la survenue d’épisodes hémorragiques et donc d’optimiser le traitement prophylactique. Avec myPKFiT, il est possible de planifier les jours d’injection en fonction du mode de vie du patient et des risques encourus, par exemple en cas de pratique sportive. « En fonction de ses caractéristiques individuelles, le patient peut présenter des modifications très variables de la durée de vie du facteur VIII. Pouvoir mesurer de façon très simple les paramètres pharmacocinétiques constitue donc un élément important. Avec myPKFiT, il est possible d’évaluer facilement la pharmacocinétique d’un patient à partir de deux échantillons sanguins a minima», indique le Dr Jean Delonca.
En pratique, à partir de ces deux prélèvements (a minima ; en général réalisés 3 heures et 24 à 32 heures après l’injection du traitement prophylactique), le médecin hématologue peut :
• reporter dans le logiciel les taux plasmatiques de FVIII,
• renseigner l’âge du patient, son poids et la sévérité de sa maladie,
• enregistrer les données d’injection (date, heure de l’injection prévue de FVIII),
• visualiser le profil pharmacocinétique individuel incluant la demi-vie du FVIII et son taux estimé à un temps donné après l’injection,
• entrer un taux cible pour le calcul automatique de la dose requise,
• choisir la fréquence d’injection la plus adaptée et générer un graphique du schéma posologique pour rester au taux cible,
• accéder à une courbe pharmacocinétique individuelle (prévoyant la décroissance des taux de FVIII en fonction du temps) et aux analyses de posologie, qu’il est possible d’imprimer et de partager avec le patient.
myPKFiT est aussi un outil de dialogue puisque le patient peut échanger de manière éclairée avec son médecin. Il est ainsi placé au cœur de sa prise en charge.
Un outil d’aide à l’information des patients
Utile pour guider le traitement prophylactique, ce logiciel a un intérêt pédagogique et éducatif. La visualisation des courbes pharmacocinétiques durant la consultation peut, en effet, être utilisée pour expliquer aux patients et à leur famille le schéma thérapeutique retenu (doses, rythme d’injections…). myPKFiT aide les patients et leur famille à mieux comprendre la maladie et les enjeux du traitement (couverture hémostatique, etc.) ; ceux-ci se sentent alors plus impliqués dans la décision thérapeutique.
Objectif « zéro saignement » : lancement de l’application myPKFiT pour les patients
Une application mobile pour un suivi partout et à tout moment
Après la mise à disposition du dispositif médical myPKFiT auprès des professionnels de santé, Shire lance l’application mobile myPKFiT (aussi qualifiée de dispositif médical) pour les patients hémophiles A.
L’application mobile myPKFiT permet au patient, partout et à tout moment, de consulter en temps réel ses estimations de taux de FVIII à partir des données d’injection, de gérer son calendrier d’injections et de suivre sa maladie en ayant un regard précis et en temps réel sur sa couverture hémostatique, de recevoir s’il le souhaite des notifications de rappels d’injection pour améliorer son suivi et son adhésion au traitement. « Avec myPKFiT, le patient peut estimer à un temps donné son taux de facteur VIII, en fonction des dernières injections. C’est une information essentielle notamment s’il a prévu tel jour de faire une activité physique. myPKFiT lui permet de faire des simulations, en fonction de la dose et de la fréquence des injections, de voir quelle sera sa couverture en termes de pourcentage de facteur VIII, ce qui peut avoir un effet rassurant », résume le Dr Jean Delonca.
En plus des injections (moment, site, dose), le patient peut également enregistrer les éventuels saignements (avec prise de photo) et le traitement ad hoc de ces épisodes et en informer son médecin pour des consultations optimisées et personnalisées.
L’application myPKFiT, en pratique
– Le médecin propose au patient d’intégrer des éléments d’information issus de son logiciel (courbe pharmacocinétique individuelle, schéma posologique pour rester au taux cible…) à l’application mobile myPKFiT afin de lui permettre de suivre son taux de FVIII et de gérer ses injections.
– Pour activer l’application :
• le médecin remet au patient le scan du QR code de son profil personnalisé (situé sur le PDF imprimé issu du logiciel médecin myPKFiT),
• le patient télécharge l’application et enregistre sa première injection directement sur l’écran d’accueil de l’application pour activer la modélisation,
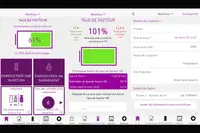
• le taux de FVIII et les zones (de confort et d’alerte) s’affichent.
L’application se met automatiquement à jour quand l’utilisateur se connecte dans les 72 heures suivant une injection.
Les injections peuvent être enregistrées, soit comme traitement prophylactique, soit comme traitement d’un saignement. Les saignements peuvent également être enregistrés dès l’écran d’accueil.
– Une fois l’application activée, le patient peut visualiser de manière pédagogique :
• son taux de facteur VIII actuel estimé,
• le temps restant dans la zone verte (de confort), le temps restant avant d’atteindre les zones jaune (prudence, le taux de FVIII estimé commence à être trop bas) ou rouge (attention, le patient risque de ne pas être totalement protégé), une fois les limites supérieures et inférieures déterminées (selon le profil pharmacocinétique),
• ses estimations futures de taux de FVIII, afin de pouvoir adapter son traitement à ses activités au cours des jours suivants,
• le nombre de jours sans saignement, ce qui encourage l’adhésion au traitement,
• un calendrier donnant un aperçu des événements passés et des événements programmés dans le futur : saignements, injections prophylactiques, traitements de saignements, injections programmées..., dans un format qui facilite le respect du schéma posologique recommandé.
Le patient peut aussi :
• recevoir des notifications, lorsque son taux estimé de FVIII est bas et qu’il est à haut risque de saignement (zone d’alerte) ou pour lui rappeler l’heure de son injection prophylactique programmée en fonction de son calendrier, dans un objectif d’amélioration de l’observance,
• enregistrer des données détaillées de ses injections et saignements (dates, heures, doses, motifs et sites d’injection, causes et localisations des saignements…) et partager les informations qu’il a renseignées avec son professionnel de santé (envoi d’un export PDF par email).
Déterminés avec le professionnel de santé, les schémas posologiques de prophylaxie personnalisée peuvent être chargés sur le compte du patient utilisateur de l’application. Si l’outil a pour but d’optimiser la prise en charge, il contribuerait également à sécuriser les patients.
Le patient, encore plus acteur de sa prise en charge et du suivi personnalisé de sa maladie
L’application myPKFiT accompagne au plus près le patient dans la prise en charge et le suivi de sa maladie, tout en favorisant son autonomie :
• elle permet au patient d’améliorer sa compréhension de sa propre couverture hémostatique et des risques associés, en fonction de l’estimation de son taux de facteur et de ses activités,
• elle favorise l’adhésion au traitement et l’implication du patient dans le suivi,
• elle améliore le dialogue entre patients et professionnels de santé (concernant la modification du schéma d’administration, la couverture au cours du temps, etc.) et pourrait optimiser les consultations en renforçant la personnalisation.
Grâce à cet outil, le patient est impliqué dans la décision thérapeutique, il participe à sa prise en charge, il gagne en autonomie et pourrait être plus observant. « Le côté ludique de cette application, le fait que les patients puissent eux-mêmes participer à la modification de leur traitement, vont faire qu’ils se sentiront plus impliqués », assure le Dr Jean Delonca. « Les deux objectifs que nous poursuivons chez Shire — faire du patient l’acteur de sa prise en charge et évoluer vers un monde sans saignement afin que les patients vivent le plus normalement possible, aient une activité professionnelle et physique quasi identique à celle de la population générale et puissent faire ce qu’ils ont envie de faire, quand ils en ont envie », conclut le directeur médical.
Hémophilie et activité physique
L’activité physique est souhaitée et recommandée chez les hémophiles, car elle leur permet d’entretenir leur masse musculaire, de préserver leur capital articulaire (articulations plus solides et plus stables), de maintenir une bonne santé en général.
Activités à encourager : celles qui ne comportent pas de risque de choc (natation, gymnastique, marche, vélo…).
Sports à éviter : ceux qui peuvent entraîner un risque hémorragique, au niveau du crâne par exemple
(judo, boxe, rugby, parachutisme, arts martiaux).
Chiffres-clés
• L’incidence annuelle de l’hémophilie A est de 1 sur 5000 naissances de garçons et la prévalence dans la population est estimée à 1/12 000.
• Si l’activité biologique du facteur de coagulation :
o est inférieure à 1 %, l’hémophilie est sévère (40-50 % des cas)
o comprise entre 1 et 5 %, l’hémophilie est modérée (10-20 % des cas)
o comprise entre 5 et 40 %, l’hémophilie est mineure (30-40 % des cas)
• L’hémophilie peut se manifester pour la première fois dès l’âge de 3 à 6 mois, ou plus tard, lorsque l’enfant commence à se déplacer
• La demi-vie du facteur VIII peut fluctuer entre 6 et 21 à 25 heures
• Le risque d’hémorragies totales et d’hémarthroses s’accroît avec le temps durant lequel le taux de facteur VIII s’abaisse en dessous de 1 %
• Indiqué en cas d’hémophilie sévère ou modérée, le traitement prophylactique consiste en 2 ou 3 injections de facteur de coagulation par semaine
• Les injections peuvent être réalisées au domicile par le patient lui-même à partir de l’âge de 12 ans, ou par un proche à partir de 4-5 ans (après une formation dans un CTH).
À propos de Shire
Shire est le leader mondial des biotechnologies au service des personnes atteintes de maladies rares et d’autres pathologies très spécifiques. Nous œuvrons au développement de médicaments qui sont à la pointe de leur catégorie. Avec de nombreux produits disponibles dans plus de 100 pays, nous couvrons différents domaines thérapeutiques, comprenant l’hématologie, l’immunologie, les neurosciences, l’ophtalmologie, les maladies de surcharge lysosomale, les maladies gastro-intestinales, la médecine interne, le système endocrinien et l’angioœdème héréditaire. Nos équipes travaillent chaque jour au service d’une mission commune : développer des traitements de pointe et les rendre accessibles à des centaines de millions de personnes à travers le monde, atteintes de maladies rares et d’autres pathologies très spécifiques, dont la qualité de vie est amoindrie par le manque de traitement efficace.
Références :
1 www.orphanet.net
2 Statistiques nationales du réseau FranceCoag : www.francecoag.org. Mise à jour du 7 février 2017.
3 Inserm : www.inserm.fr/information-en-sante/dossiers-information/hemophilie
4 Orphanet :
a. www.orpha.net/consor/cgi-bin/OC_Exp.php?Lng=FR&Expert=448
b. L’hémophilie Encyclopédie Orphanet Grand Public : www.orpha.net/data/patho/Pub/fr/Hemophilie- FRfrPub646v01.pdf
5 Alliance maladies rares : www.alliance-maladies-rares. org/association/nos-partenaires/nous-connaitre/les-
associations-membres/association-francaise-des-hemophiles/
6 Collins PW, Björkman S, Fischer K, et coll. Factor VIII requirement to maintain a target plasma level in the
prophylactic treatment of severe hemophilia A: influences of variance in pharmacokinetics and treatment regimens. J Thromb Haemost. 2010;8 (2) : 269-75.
7 Collins PW, Blanchette VS, Fischer K, et al. Break-through bleeding in relation to predicted factor VIII levels in
patients receiving prophylactic treatment for severe hemophilia A. J Thromb Haemost. 2009;7(3):413-20.
8 Valentino LA. Considerations in individualizing prophylaxis in patients with haemophilia A. Hemophilia.
2014;20(5):607-615.
9 Manuel d’utilisation myPKFiT site internet pour les professionnels de santé — version 2.0 — Baxalta Inc. 2016.
10 Manuel d’utilisation myPKFiT application mobile — version 2.0 — Baxalta Inc. 2018.
Descripteur MESH : Patients , Vie , Santé , Injections , Risque , Thérapeutique , Temps , Compréhension , Pharmacocinétique , Maladie , Logiciel , Qualité de vie , Physique , Maladies rares , Accidents , Articulations , Personnes , Population , France , Chromosome X , Famille , Choc , Nature , Arts martiaux , Aire sous la courbe , Internet , Prévalence , Extraction dentaire , Adulte , Éléments , Réseau , Prévention des accidents , Précis , Statistiques , Paris , Crâne , Histoire , Attention , Boxe , Sports , Gymnastique , Objectifs , Soins , Médecine interne , Médecine , Neurosciences , Génétique , Natation , Phénotype , Mutation

